Rund 12% der Bevölkerung leiden unter Migräne. Die neurologische Erkrankung ist weltweit der zweithäufigste Grund für ein Leben mit Behinderung und der häufigste Grund für Menschen unter 50 Jahren. Eine gute Prophylaxe reduziert das Risiko der Krankheitsprogression und kann zur Remission der Erkrankung führen. Hierfür stellen CGRP-(Rezeptor)-Antikörper und die Neuromodulation mit Cefaly zwei wichtige Säulen dar.
Die Migräne ist eine neurologische Erkrankung, unter der ca. 12% der Bevölkerung leidet [1]. Sie tritt bei Frauen etwa dreimal so häufig auf wie bei Männern. Migräne ist weltweit der zweithäufigste Grund nach unteren Rückenschmerzen für ein Leben mit Behinderung und der häufigste Grund für Menschen unter 50 Jahren [2]. Menschen mit chronischer Migräne verlieren etwa 14% ihrer jährlichen Produktivität, und 20% davon berichten, dass sie nicht in der Lage sind, Aufgaben zu erfüllen, die für ihre Arbeit erforderlich sind [3]. Jährlich entstehen dadurch sowohl für Betroffene als auch für Arbeitgeber und das Gesundheitssystem erhebliche Kosten.
Die Essenz der Erkrankung ist, dass bei betroffenen Patienten lebenslang eine Veranlagung zu Migräneattacken besteht. Der Pathomechanismus der Attacke ist nicht vollständig aufgeklärt. Die wichtigste Erkenntnis der letzten Jahre ist, dass die Kopfschmerzattacke selbst am ehesten mit einer Dysfunktion diencephaler und mesencephaler Strukturen assoziiert ist, namentlich dem Hypothalamus und dem periaquäduktalen Grau [4]. Unmittelbar vor Attacken kommt es durch die Fehlfunktion dieser Areale zu einer Verarbeitungsstörung sensorischen Inputs, v.a. sensibel aus den Bereichen des N. trigeminus, verantwortlich für die Schmerzen, aber auch aus anderen Bereichen wie dem gastrointestinalen (Nausea, Erbrechen) oder dem visuellen/auditiven (Photophobie/Phonophobie) System [5]. Neben diesem zentralen Mechanismus hat sich zuletzt das Neuropeptid calcitonin gene-related peptide (CGRP), als hoch relevant erwiesen. Dieses ist in Migräneattacken im Jugularvenenblut erhöht und fällt nach erfolgreicher Therapie mit Sumatriptan wieder ab [6,7]. Weiterhin können Infusionen mit CGRP bei Patienten mit Migräne Kopfschmerzattacken triggern, und die Blockade von CGRP-Rezeptoren kann Migräneattacken stoppen [8,9]. Die Entwicklung von Antikörpern gegen das CGRP-System hat im letzten Jahrzehnt die Migränetherapie revolutioniert, und die oralen CGRP-Rezeptor-Blocker werden auch in den nächsten Jahren in der Schweiz zunehmende Bedeutung erhalten.
Ziel dieses Artikels ist eine Übersicht über die gängigen und neuartigen Verfahren zur Migränetherapie mit einer Betonung auf die Herausforderungen bei der Anwendung im Alltag.
Therapie
Die Therapie der Migräne besteht aus zwei Hauptsäulen: die bedarfsgerecht eingenommene Akuttherapie mit dem Ziel der Linderung des Migräneschmerzes sowie die regelmässig eingenommene Basistherapie mit dem Ziel der Reduktion der Frequenz und auch der Intensität bzw. Dauer der Migräneattacken.
Akuttherapie: Bei leichteren Attacken sind weiterhin NSAR ausreichend, während für mittlere bis starke Migräneattacken bzw. bei fehlendem Ansprechen Triptane eingesetzt werden, welche spezifische Migränemedikamente darstellen. Die Triptane unterscheiden sich untereinander hinsichtlich Wirkstärke, Wirkdauer und Applikationsart. Stark wirksam und mit schnellem Wirkeintritt sind beispielsweise subkutanes und nasales Sumatriptan, nasales Zolmitriptan und Eletriptan bzw. Rizatriptan. Bei langanhaltenden Attacken sind Präparate mit langer Halbwertszeit, wie Naratriptan, Frovatriptan oder die Kombination eines Triptans mit dem lang wirksamen NSAR Naproxen eine Option. Almogran, Naratriptan und Frovatriptan sind Präparate mit einem günstigen Nebenwirkungsprofil.
Die teilweise vasokonstriktorisch bedingten Nebenwirkungen sind: passagerer Blutdruckanstieg, selten Durchblutungsstörungen, EKG-Veränderungen, Herzrhythmusstörungen, Parästhesien der Extremitäten, Kältegefühl bis zu dem in der klinischen Praxis sehr seltenen Raynaud-Syndrom, Schwindel, Benommenheit bzw. Müdigkeit und Flush.
Wichtig ist, dass ein Medikamentenübergebrauchskopfschmerz vermieden wird. Dieser liegt gemäss ICHD-3 Klassifikation vor bei Patienten, die chronischen Kopfschmerz haben, also mehr als 15 Kopfschmerztage mit Medikamenteneinnahme an >10 Tagen/Monat für Triptane oder >15 Tagen/Monat für Analgetika.
Basistherapie: Die Basistherapie besteht aus medikamentösen und nicht-medikamentösen Massnahmen. Wichtig zu erwähnen ist, dass eine optimale Basistherapie das Risiko der Krankheitsprogression signifikant reduzieren kann (von 6,8% auf 1,9%) [10].
Nicht-medikamentöse Massnahmen
Hierbei handelt es sich um einen gesunden Lebensstil mit regelmässigen Schlafens- und Essenszeiten, ausgewogener Ernährung und regelmässigem Sport (mind. 3x30Min pro Woche). Neue Studien zeigen sogar, dass Krafttraining leicht wirksamer ist als Ausdauersport [11]. Auch Entspannungsverfahren wie die progressive Muskelrelaxation nach Jakobson sind wichtig und können eine Reduktion der Migränetage um über 40% erreichen [12]. Die Instruktion ist einfach und kann von Physiotherapeuten vermittelt oder auch im Selbststudium erlernt werden (z.B. via InselApp oder auf Youtube). Weitere nicht medikamentöse Massnahmen sind Biofeedback, psychologische Schmerztherapie und ggf. kognitive Verhaltenstherapie.
Medikamentöse Massnahmen
Der Einsatz einer medikamentösen Prophylaxe wird individuell je nach Leidensdruck und Einstellung des Patienten entschieden. Mehr als vier Migräneattacken pro Monat, langanhaltende Attacken, unzureichendes Ansprechen auf Akuttherapie, Medikamentenübergebrauch, häufige migränebedingte Fehltage sowie ein stattgehabter migränoser Infarkt stellen die typische Indikation für den Beginn einer medikamentösen Basistherapie dar (Abb. 1). Wichtig für die Wahl der Therapie ist die Berücksichtigung der Komorbiditäten des Patienten zur Vorbeugung von unerwünschten Nebenwirkungen. Im Fall eines Kinderwunsches sind in Absprache mit dem Gynäkologen bzw. der Gynäkologin typischerweise Betablocker sowie Amitriptylin möglich. Bei den anderen Substanzen wie Topiramat oder Flunarizin sollte bei Frauen im gebärfähigen Alter immer auch auf die Wichtigkeit der Kontrazeption hingewiesen werden.
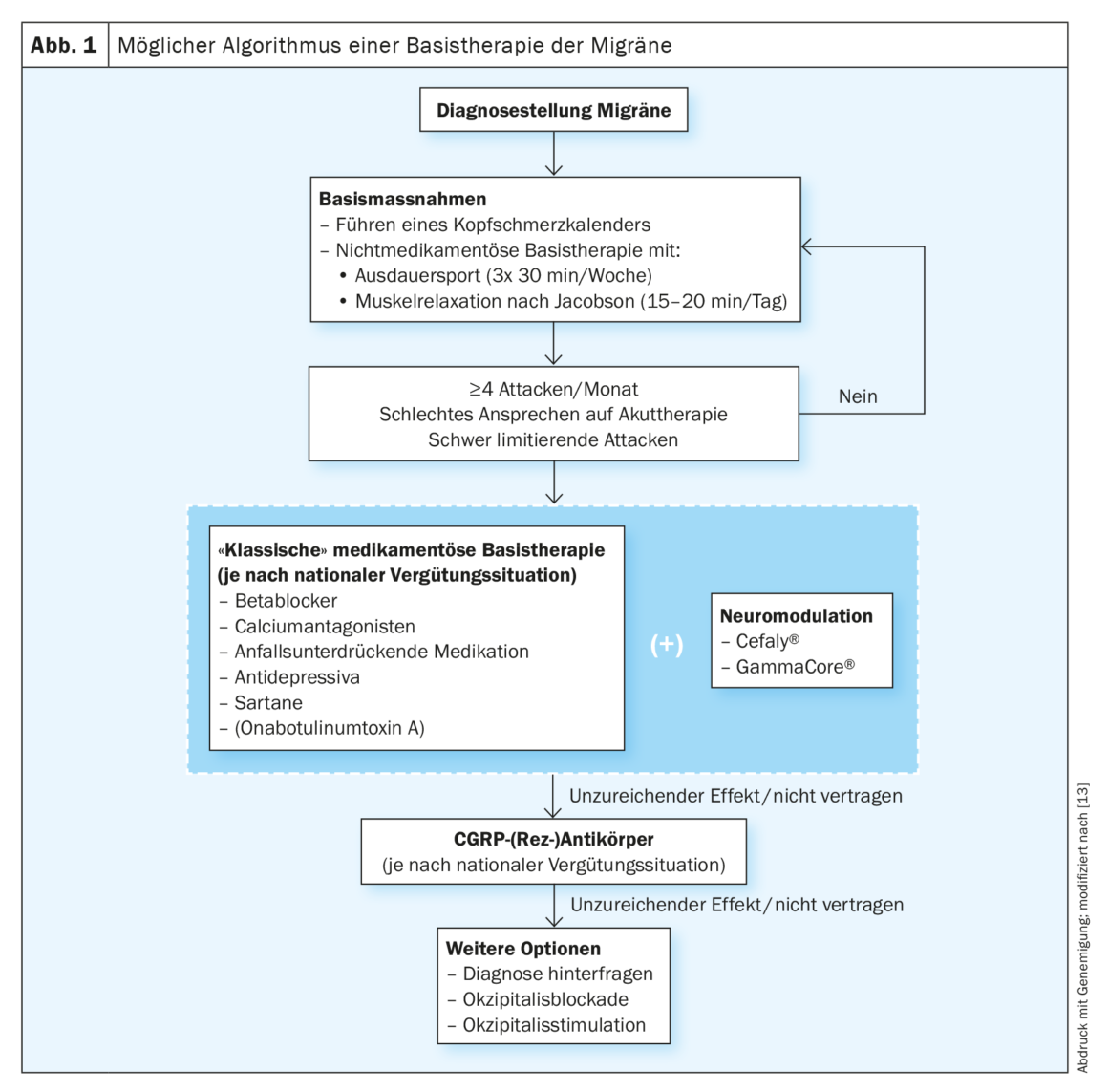
Am besten durch kontrollierte Studien belegt, ist die prophylaktische Wirkung der Betablocker Propranolol und Metoprolol, des Kalziumantagonists Flunarizin, der Antikonvulsiva Valproinsäure und Topiramat und des Antidepressivums Amitriptylin. Auch das Antihypertensivum Candesartan und das SNRI Venlafaxin stellen gute Alternativen dar. Wichtig sind ein langsames Eindosieren sowie die Aufklärung über Nebenwirkungen.
Die Basistherapie sollte über drei Monate eingenommen und die Wirksamkeit anhand des Kopfschmerzkalenders evaluiert werden. Bei Wirksamkeit über mindestens sechs Monate kann eine vorsichtige Reduktion versucht werden. Onabotulinumtoxin Typ A ist in der Schweiz nicht zur Therapie der Migräne zugelassen, kann aber im Einzelfall über eine Kostengutsprache beantragt werden. Es zeigte sich in den beiden Phase-III-Studien PREEMPT 1 und 2 effektiver als Placebo in der Prophylaxe der chronischen Migräne (mittlere Reduktion der monatlichen Kopfschmerztage um 8,4 unter Onabotulinumtoxin Typ A vs. 6,6 unter Placebo; p<0,001) [14]. Gemäss PREEMPT-Schema erhält der Patient 31 Injektionen an sieben spezifischen Kopf- und Nackenmuskelbereichen mit einer Mindestdosierung von 155 Einheiten. Der Abstand zwischen den Behandlungen beträgt drei Monate.
Hindernisse
Ein häufiges Problem bei Migränepatienten ist die «lange Reise» des Patienten bis zur Diagnosestellung bzw. Behandlung. Viele Patienten versuchen zunächst Medikamente aus ihrem Bekanntenkreis oder Präparate, die sie im Internet finden oder von ihrem Apotheker erhalten. Wenn im Verlauf der Leidensdruck steigt, wird der Hausarzt aufgesucht. Es kann Monate bis Jahre dauern bis der Patient zu einem Neurologen oder einem auf Kopfschmerzen spezialisierten Neurologen überwiesen wird. Dieser lange Leidensweg ist oftmals auch mit Angst, Hoffnungslosigkeit, Frustration und Skeptizismus gegenüber Medikamenten verbunden.
Ein weiteres Problem stellt der geringe Anteil Patienten dar, die eine Basistherapie erhalten. Trotz ärztlicher Beratung erhielten in einer Studie nur 26% der Patienten eine Basistherapie, die Anspruch auf eine solche haben. Zirka zwei Drittel der Patienten mit chronischer Migräne haben noch nie eine Basistherapie erhalten [15]. Erschwerend kommt hinzu die geringe Adhärenz. Etwa 80% der Patienten mit chronischer Migräne brechen die Therapie im ersten Jahr ab [16]. Ähnliche Zahlen ergeben sich auch für Patienten mit episodischer Migräne [17]. Die Hauptgründe dafür sind unklar, aber fehlende Hoffnung, dass das Medikament überhaupt wirkt, die Sorge vor Nebenwirkungen, die Kosten sowie ein gewisser Skeptizismus von jungen Menschen gegen eine täglich eingenommene orale Medikation sind sicherlich relevant.
Optionen und neuere Erkenntnisse
Wichtig ist, dass die primären Ansprechpersonen für die Patienten (Apotheker, Hausarzt) die komplexeren Fälle frühzeitig erkennen. Schwerer betroffene Patienten haben gehäufte Migräneattacken oder sogar einen Dauerkopfschmerz; sie benötigen regelmässig Schmerzmitteln und haben damit ein erhöhtes Chronifizierungsrisiko oder sprechen, wenn überhaupt, nur vorübergehend auf die konventionellen Analgetika bzw. Basistherapeutika an.
Antikörpertherapie: Ein grosser Fortschritt bei der Behandlung der Migräne ist die Anwendung der monoklonalen Antikörper, welche seit wenigen Jahren in der Schweiz zugelassen sind. Diese Medikamente unterliegen einer Limitatio. Sie dürfen bei therapierefraktären Migräne-Patienten mit hochfrequenter episodischer (≥8 Migränetage/Monat) oder chronischer Migräne angewendet werden. Therapierefraktär ist in diesem Zusammenhang definiert als eine erfolglose oder aufgrund von Nebenwirkungen abgebrochene vorangegangene Behandlung mit mindestens zwei der folgenden Medikamente: Betablocker (Metoprolol oder Propranolol), Amitriptylin, anfallsunterdrückende Medikation (v.a. Topiramat, aber auch Valproat) und Kalziumantagonisten (v.a. Flunarizin). Alternativ müssen Kontraindikationen für alle vier Gruppen vorliegen. Vorteile dieser Substanzen sind der schnelle Wirkeintritt, die gute Wirksamkeit und Verträglichkeit und die einfache Anwendung (1× pro Monat, bei einigen 1× alle drei Monate). Damit ist eine bessere Adhärenz verglichen mit den oralen Therapeutika zu erwarten. Die Hauptnebenwirkungen sind Obstipation und lokale Reaktion im Bereich der Injektionsstelle. Nachteile der Therapie sind sicherlich die recht hohen Kosten, die oben beschriebene komplexe Limitatio und natürlich die relativ kurze Zeit, die die Präparate erhältlich sind mit entsprechend geringer Erfahrung. Beispielsweise fand sich in den letzten Jahren ausserhalb der Phase-III-Studien, dass die CGRP-Antikörper vermutlich ein Raynaud-Syndrom teilweise deutlich verschlechtern können, und dass bei manchen Patienten mit arterieller Hypertonie oder Kardiopathie eine genauere Überwachung notwendig sein könnte.
Konkret handelt es sich bei diesen Medikamenten um Antikörper gegen den CGRP-Rezeptor (Erenumab) oder gegen den CGRP-Liganden selbst (Eptinezumab, Fremanezumab, Galcanezumab). Erenumab, Fremanezumab und Galcanezumab werden subkutan verabreicht, Eptinezumab intravenös.
Da Eptinezumab intravenös verabreicht wird, wirkt es besonders schnell. Wenn die Prophylaxe beispielsweise innerhalb einer Attacke begonnen wird, sind 46,6% der Patienten innerhalb von vier Stunden schmerzfrei im Vergleich zu 26,4% in der Placebo-Gruppe [18]. Zu betonen ist, dass Eptinezumab nicht zur Akuttherapie der Migräne zugelassen ist. Limitierend ist möglicherweise der notwendige Spitalbesuch für die Infusion. Fremanezumab zusammen mit Eptinezumab bieten den Vorteil der einmaligen Anwendung über drei Monate, im Gegensatz zu Erenumab und Galcanezumab, welche 1× Monat gespritzt werden. Bei Galcanezumab soll ein Loading mit zweifacher Dosierung bei der ersten Applikation erfolgen. Erenumab bietet den Vorteil der möglichen Dosiserhöhung (von 70 mg auf 140 mg).
Neuromodulation: Bei den neuromodulatorischen Ansätzen wirken elektrische und/oder magnetische Stimulationsverfahren direkt auf die Nervenzellen im Gehirn oder periphere Nerven mit dem Ziel der Erhöhung der Schmerzschwelle und damit Reduktion der Häufigkeit und Intensität des Schmerzempfindens. Vorteil der Neuromodulation, insbesondere der nicht-invasiven Verfahren, ist das Fehlen systemischer Nebenwirkungen und die damit anzunehmende bessere Toleranz im Vergleich zu den oralen Medikamenten. Zudem können diese Verfahren täglich angewendet werden als Akuttherapie ohne Gefahr eines Übergebrauchkopfschmerzes.
Man unterscheidet invasive Verfahren, bei denen ein Stimulator mit Elektroden implantiert wird, und nicht invasive Verfahren, bei denen Geräte an der Haut vom Patienten selbst eingesetzt werden. Bei den nichtinvasiven Verfahren wird in diesem Artikel auf die transdermale Stimulation des Nervus vagus und des N. supraorbitalis eingegangen. Invasive Verfahren wie die Nervus-occipitalis-Stimulation sollten therapieresistenten Fällen vorbehalten sein und nur nach interdisziplinärer Evaluation durch Neurologen mit Neurochirurgen und den Kollegen der Psychosomatik angewandt werden.
Transkutane Stimulation des N. supraorbitalis (Cefaly®)
Nach Anbringen einer selbstklebenden Elektrode auf der Stirn wird Cefaly magnetisch an die Elektrode angeschlossen. Durch die Elektrode werden dann präzise Mikroimpulse an den supraorbitalen und supratrochlearen Äste des Nervus ophthalmicus gesendet, um entweder die Kopfschmerzen bei einem Migräneanfall zu lindern (akute Behandlung) oder um zukünftige Migräneanfälle zu verhindern (präventive Behandlung).
Das Gerät bietet zwei verschiedene Programme: Ein Programm für die Basistherapie, welche täglich angewendet wird für ca. 20 Minuten (niederfrequente Stimulation) und ein zweites Programm für die Akut-therapie über 60 Minuten (hochfrequente Stimulation). Zahlreiche Studien unterstützen den Effekt von Cefaly bei Migräne. Eine sham-kontrollierte Doppelblindstudie zum Beispiel zeigte eine 19% Reduktion der Migräneattacken in der Verum Gruppe im Vergleich zu 3% Reduktion in der Placebo Gruppe [19]. In einer amerikanischen offenen Pilotstudie ergab sich eine 57,1%-ige Reduktion der mittleren Schmerzintensität nach einstündiger Anwendung des Geräts [20].
In der Schweiz wird das Gerät zunächst von den Patienten direkt vom Hersteller erworben. Sollte der Patient nicht davon profitieren, kann er es zurückschicken und erhält eine teilweise Rückerstattung des Kaufpreises. Bei Wirksamkeit ist eine teilweise Rückerstattung als TENS-Gerät per Rezept möglich.
Transkutane Stimulation des N. vagus (GammaCore®)
Die Vagusnervstimulation wird seit längerem zur unterstützenden Therapie von schwer behandelbaren Epilepsien und Depression eingesetzt. Es wurde bereits gezeigt, dass bei chronischen Schmerzen häufig der Vagusnerv weniger aktiv ist und damit der Ausgleich zwischen Sympathikus und Parasympathikus gestört ist. Gelingt es, den Parasympathikus zu stimulieren, spüren die Patienten weniger Schmerzen.
Einige Studien zeigten einen Effekt beim Clusterkopfschmerz [21]. Ausserdem konnte gezeigt werden, dass die Vagusnervstimulation die kortikale Streudepolarisation (Cortical Spreading Depression)hemmt, welche möglicherweise der Migräneaura zugrunde liegt [22]. Offene Studien lassen einen Effekt auch für die Behandlung von akuten Migräneattacken vermuten [23,24]. Zwei grosse, placebo-kontrollierte, doppelblinde Studien zeigten allerdings nur eine geringe, nicht-signifikante Reduktion der Migränetage gegenüber Sham-Stimulation [25,26].
Die Vagusnerv-Stimulation mit gammaCore® erfolgt in der Regel 2× pro Tag (empfohlen: morgens und abends mit je 2–3 Stimulationen). Diese dauern jeweils 90 Sek. Das Gerät ist ab der ersten Aktivierung maximal 31 Kalendertage verwendbar und ermöglicht bis zu 300 Stimulationen. Somit besteht über die regelmässige Prophylaxe (ca. 186 Stimulationen) hinaus genügend Kapazität für (akuttherapeutische) Reservestimulationen.
Momentan ist das Gerät nicht in der Schweiz verfügbar, und die aktuelle Studienlage ist bisher nicht überzeugend. Für den Einzelfall kann es aber als individueller Heilversuch beispielsweise aus UK bestellt werden. Kontraindikationen für das Cefaly Gerät und das Gamma-Core stellen implantierte elektronische Geräte wie Herzschrittmacher dar.
Prävention im Alltag
Monoklonale CGRP-Antikörper können beitragen, ungedeckte Bedürfnisse in der Migräneprävention im Alltag zu erfüllen. Die Erkenntnisse aus dem Praxisalltag (Real-World-Evidence Data) zeigen ein vergleichbares Wirksamkeits- und Sicherheitsprofil im Vergleich zu den randomisierten Zulassungsstudien. Erwähnenswert sind die Daten aus der Garlit-Studie [27]. Es handelt sich um eine multizentrische, prospektive Beobachtungskohortenstudie aus Italien mit 163 Teilnehmern mit hochfrequenter episodischer Migräne (HFEM, 8–14 Migränetage pro Monat) und chronischer Migräne (CM). Die Patienten erhielten eine Loading Dose von Galcanezumab 240 mg s/c, gefolgt von 120 mg s/c monatlich.
Nach sechs Monaten verringerten sich die monatlichen Migränetage bei HFEM-Patienten um acht Tage und die Migränekopfschmerztage bei CM-Patienten um 13 Tage. Zudem kam es zu einer raschen Reduktion der Migränetage bereits im ersten Behandlungsmonat bei über 60% der Patienten, welche über die sechs Monate anhielt. 76,5% der HFEM und 63,5% der CM-Patienten erreichten eine 50%-ige Ansprechrate über drei aufeinanderfolgende Monate. Zudem zeigt sich ein günstiges Verträglichkeitsprofil mit 10,3% unerwünschten Ereignissen über sechs Monate, am häufigsten Obstipation und Reaktionen an der Injektionsstelle. Es wurden keine schwerwiegenden unerwünschten Ereignisse gemeldet.
In einer Real-World-Studie mit 26 Patienten mit chronischer Migräne mit und ohne Kopfschmerz bei Medikamentenübergebrauch, bei denen mindestens drei präventive Therapien versagt hatten, zeigte sich für 62% der Patienten ein Wechsel von chronischer zu episodischer Migräne im ersten Behandlungsjahr [28]. Im Gegensatz dazu liegt die Wahrscheinlichkeit einer spontanen Remission bei nur 26,1% über zwei Jahre. Die oben genannten Daten beziehen sich auf Galcanezumab, die Erfahrung aus dem klinischen Alltag ergibt allerdings vergleichbare Ergebnisse für alle Antikörperpräparate.
Zusammenfassung
Aktuell gibt es eine grosse Zahl an wirksamen Therapieverfahren zur Behandlung der Migräne. Man unterscheidet Akuttherapie und Basistherapie sowie medikamentöse und nichtmedikamentöse Verfahren. Eine gute Prophylaxe reduziert das Risiko der Krankheitsprogression und kann zur Remission der Erkrankung führen. Leider erhält nur ein kleiner Teil der Migränepatienten eine Basistherapie, obwohl diese indiziert wäre. Und die Patienten, die eine Prophylaxe erhalten zeigen oftmals eine geringe Medikamenten-Adhärenz. Dies zu verbessern ist eine gemeinsame Aufgabe aller an der Versorgung von Migränepatienten beteiligten Berufsgruppen. Obwohl erst seit wenigen Jahren in der Schweiz zugelassen, stellen die CGRP-(Rezeptor)-Antikörper bereits eine wichtige Säule der Migränetherapie dar. Eine vielversprechende Ergänzung der regelmässig zu praktizierenden nicht-medikamentöse Prophylaxe ist die Neuromodulation mit Cefaly®.
Take-Home-Messages
- Die Migräne ist einer der häufigsten Gründe für Behinderung bei Menschen unter 50 Jahren.
- Eine gute Prophylaxe reduziert das Risiko der Krankheitsprogression und kann zur Remission der Erkrankung führen.
- Die CGRP-(Rezeptor)-Antikörper und die Neuromodulation mit Cefaly stellen zwei wichtige Säulen der Migränetherapie dar.
Literatur:
- Burch RC, Buse DC, Lipton RB: Migraine: Epidemiology, Burden, and Comorbidity. Neurol Clin 2019 Nov; 37(4): 631–649. doi: 10.1016/j.ncl.2019.06.001. Epub 2019 Aug 27. PMID: 31563224.
- Steiner TJ, Stovner LJ, Vos T, et al.: (2018). Migraine is the first cause of disability in those under 50: will health politicians now take notice?. The journal of headache and pain, 19(1), 17. doi:10.1186/s10194-018-0846-2
- Migraine and Disability, Headache and Migraine Policy Forum, https://static1.squarespace.com/static/
5886319ba5790a66cf05d235/t/5c65958215fcc0538b9c85de/1550161282886/HMPF_Migraine+%26+Disability+Graphic_Feb+2019.pdf - Maniyar FH, Sprenger T, Monteith T, et al.: Brain activations in the premonitory phase of nitroglycerin-triggered migraine attacks. Brain 2014 Jan; 137(Pt 1): 232–241. doi: 10.1093/brain/awt320. Epub 2013 Nov 25. PMID: 24277718.
- Goadsby PJ, Holland PR, Martins-Oliveira M, et al.: Pathophysiology of Migraine: A Disorder of Sensory Processing. Physiol Rev 2017 Apr; 97(2): 553–622. doi: 10.1152/physrev.00034.2015. PMID: 28179394; PMCID: PMC5539409.
- Goadsby PJ, Edvinsson L, Ekman R. Vasoactive peptide release in the extracerebral circulation of humans during migraine headache. Ann Neurol. 1990 Aug;28(2):183-7. doi: 10.1002/ana.410280213. PMID: 1699472.
- Goadsby PJ, Edvinsson L: The trigeminovascular system and migraine: studies characterizing cerebrovascular and neuropeptide changes seen in humans and cats. Ann Neurol 1993 Jan; 33(1): 48–56. doi: 10.1002/ana.410330109. PMID: 8388188.
- Lassen LH, Haderslev PA, Jacobsen VB, et al.: CGRP may play a causative role in migraine. Cephalalgia 2002 Feb; 22(1): 54–61. doi: 10.1046/j.1468-2982.2002.00310.x. PMID: 11993614.
- Olesen J, Diener HC, Husstedt IW, et al., BIBN 4096 BS Clinical Proof of Concept Study Group: Calcitonin gene-related peptide receptor antagonist BIBN 4096 BS for the acute treatment of migraine. N Engl J Med. 2004 Mar 11;350(11): 1104–1110. doi: 10.1056/NEJMoa030505. PMID: 15014183.
- Lipton RB, Fanning KM, Serrano D, et al.: Ineffective acute treatment of episodic migraine is associated with new-onset chronic migraine. Neurology 2015 Feb 17; 84(7): 688–695. doi: 10.1212/WNL.0000000000001256. Epub 2015 Jan 21. PMID: 25609757; PMCID: PMC4336107.
- Woldeamanuel YW, Oliveira ABD: What is the efficacy of aerobic exercise versus strength training in the treatment of migraine? A systematic review and network meta-analysis of clinical trials. J Headache Pain 23, 134 (2022).
https://doi.org/10.1186/s10194-022-01503-y - Meyer B, Keller A, Wöhlbier HG, et al.: Progressive muscle relaxation reduces migraine frequency and normalizes amplitudes of contingent negative variation (CNV). J Headache Pain 17, 37 (2016). https://doi.org/10.1186/s10194-016-0630-0
- Frank J, Schankin CJ: Aktuelle und zukünftige Therapieoptionen bei Migrne: ein Update. Neuro Aktuell 2021;5: 23–30. (Die Abbildung mit Genehmigung reproduziert).
- Dodick DW, Turkel CC, DeGryse RE, PREEMPT Chronic Migraine Study Group, et al.: OnabotulinumtoxinA for treatment of chronic migraine: pooled results from the double-blind, randomized, placebo-controlled phases of the PREEMPT clinical program. Headache 2010 Jun; 50(6): 921–936.
doi: 10.1111/j.1526-4610.2010.01678.x. Epub 2010 May 7. PMID: 20487038. - Lipton RB, Nicholson RA, Reed ML, et al.: Diagnosis, consultation, treatment, and impact of migraine in the US: Results of the OVERCOME (US) study. Headache 2022 Feb; 62(2): 122–140. doi: 10.1111/head.14259. Epub 2022 Jan 25. PMID: 35076091; PMCID: PMC9305407.
- Hepp Z, Dodick DW, Varon SF, et al.: Adherence to oral migraine-preventive medications among patients with chronic migraine. Cephalalgia. 2015 May; 35(6): 478–488. doi: 10.1177/0333102414547138. Epub 2014 Aug 27. PMID: 25164920.
- Berger A, Bloudek LM, Varon SF, Oster G: Adherence with migraine prophylaxis in clinical practice. Pain Pract 2012 Sep;12(7): 541–549. doi: 10.1111/j.1533-2500.2012.00530.x. Epub 2012 Feb 2. PMID: 22300068.
- Winner, et al.: Effects of Intravenous Eptinezumab vs Placebo on Headache Pain and Most Bothersome Symptom When Initiated During a Migraine Attack: A Randomized Clinical Trial. JAMA 2021; 325(23): 2348–2356.
- Schoenen J, Vandersmissen B, Jeangette S, et al.: Migraine prevention with a supraorbital transcutaneous stimulator. A randomized controlled trial. Neurology Feb 2013, 80(8); 697–704;
DOI: 10.1212/WNL.0b013e3182825055 - Chou DE, Gross GJ, Casadei CH, Yugrakh MS: External Trigeminal Nerve Stimulation for the Acute Treatment of Migraine: Open-Label Trial on Safety and Efficacy. Neuromodulation 2017 Oct; 20(7): 678–683. doi: 10.1111/ner.12623. Epub 2017 Jun 5. PMID: 28580703.
- Gaul C, Diener HC, Silver N, Magis D, et al.: Non-invasive vagus nerve stimulation for PREVention and Acute treatment of chronic cluster headache (PREVA): A randomised controlled study. Cephalalgia. 2016 May;36(6):534-46. doi: 10.1177/0333102415607070. Epub 2015 Sep 21. PMID: 26391457; PMCID: PMC4853813.
- Chen SP, Ay I, de Morais AL, et al.: Vagus nerve stimulation inhibits cortical spreading depression. Pain 2016; 157: 797–805
- Barbanti P, Grazzi L, Egeo G, et al.: Noninvasive vagus nerve stimulation for acute treatment of high-frequency and chronic migraine: an open-label study. The journal of headache and pain 2015; 16: 61. 11.
- Goadsby PJ, Grosberg BM, Mauskop A, et al.: Effect of noninvasive vagus nerve stimulation on acute migraine: an openlabel pilot study. Cephalalgia: an international journal of headache 2014; 34: 986–999.
- Diener HC, Goadsby PJ, Ashina M, et al.: Non-invasive vagus nerve stimulation (nVNS) for the preventive treatment of episodic migraine: The multicentre, double-blind, randomised, sham-controlled PREMIUM trial. Cephalalgia 2019 Oct; 39(12): 1475–1487. doi: 10.1177/0333102419876920. Epub 2019 Sep 15. PMID: 31522546; PMCID: PMC6791025.
- Silberstein SD, Calhoun AH, Lipton RB, EVENT Study Group, et al.: Chronic migraine headache prevention with noninvasive vagus nerve stimulation: The EVENT study. Neurology 2016 Aug 2; 87(5): 529–38. doi: 10.1212/WNL.0000000000002918. Epub 2016 Jul 13. PMID: 27412146; PMCID: PMC4970666.
- Vernieri F, Altamura C, Brunelli N, et al.: Galcanezumab for the prevention of high frequency episodic and chronic migraine in real life in Italy: a multicenter prospective cohort study (the GARLIT study). J Headache Pain 2021 May 3;22(1): 35. doi: 10.1186/s10194-021-01247-1. PMID: 33941080; PMCID: PMC8091153.
- Vaghi G, Bitetto V, De Icco R, et al.: Real life experience of one year treatment with galcanezumab in chronic migraine with and without medication overuse headache. Cephalalgia 2021; 41: 162.
InFo NEUROLOGIE & PSYCHIATRIE 2023; 21(2): 6–10
Autoren
- Prof. Dr. med. Christoph J. Schankin
- Leonidas D. Panos
Publikation
- INFO NEUROLOGIE & PSYCHIATRIE




Comments are closed.