Für Patienten mit chronischer Herzinsuffizienz stehen heutzutage eine Reihe von Therapiemöglichkeiten zur Verfügung. Nicht immer ist es einfach, die richtige Wahl zu treffen.
Fortschritte in der medizinischen Behandlung, vor allem des akuten Koronarsyndroms, führten in jüngerer Vergangenheit zu einem stetigen Anstieg der Prävalenz der chronischen Herzinsuffizienz – aktuell sind etwa 26 Millionen weltweit und ca. 200’000 Patienten in der Schweiz betroffen. Da der Krankheitsverlauf nur hinausgezögert, die Grunderkrankung aber nicht rückgängig gemacht werden kann, erreichen immer mehr, auch jüngere Patienten ein schwer symptomatisches Stadium mit stark eingeschränkter Lebensqualität und hoher Einjahres-Sterblichkeit.
Die Entscheidung welcher Patient, wann, welche weiterführende Therapie erhalten soll, zählt hier zu den schwierigsten Aufgaben. Eine Herztransplantation bietet meist eine sehr gute Lebensqualität und die Patienten haben ein hervorragendes Langzeitüberleben (nach 12,4 Jahren leben noch 50% der transplantierten Patienten [ISHLT]). Aufgrund des weiterhin bestehenden Mangels an Spenderorganen kann diese Behandlung jedoch nur wenigen ausgewählten und meist jüngeren Patienten angeboten werden. Bei einer durchschnittlichen Wartezeit von 1–2 Jahren ist die Transplantation zudem keine Option in der Akutsituation; als langfristige Therapiealternative (Destination-Therapy) oder Überbrückung (Bridge-to-Transplant) kommt dann eine mechanische Kreislaufunterstützung mit einem Linksherzunterstützungssystem (LVAD) in Frage. T. Carrel und D. Reineke haben in der letzten Ausgabe einen guten Überblick über mechanische Kreislaufunterstützung bei akuter und chronischer Herzinsuffizienz gegeben.
Wer profitiert von einem Kunstherz und wie erkennt man den optimalen Zeitpunkt für eine solche Therapie?
In den letzten Jahren wurden vor allem Patienten in den INTERMACS (IM) Kategorien 1–3 für die Implantation eines Linksventrikulären Assistdevice (LVAD) in Betracht gezogen (Tab. 1). Das heisst Patienten mit kritischem kardiogenem Schock (IM Profil 1), rascher Verschlechterung trotz maximaler intensivmedizinischer Therapie (IM Profil 2) oder solche, die nicht von der Therapie mit Inotropika entwöhnt werden können (IM Profil 3); also jene Patienten für die ein Überleben ausserhalb des Krankenhauses ohne weiterführende Therapie nicht möglich gewesen wäre.
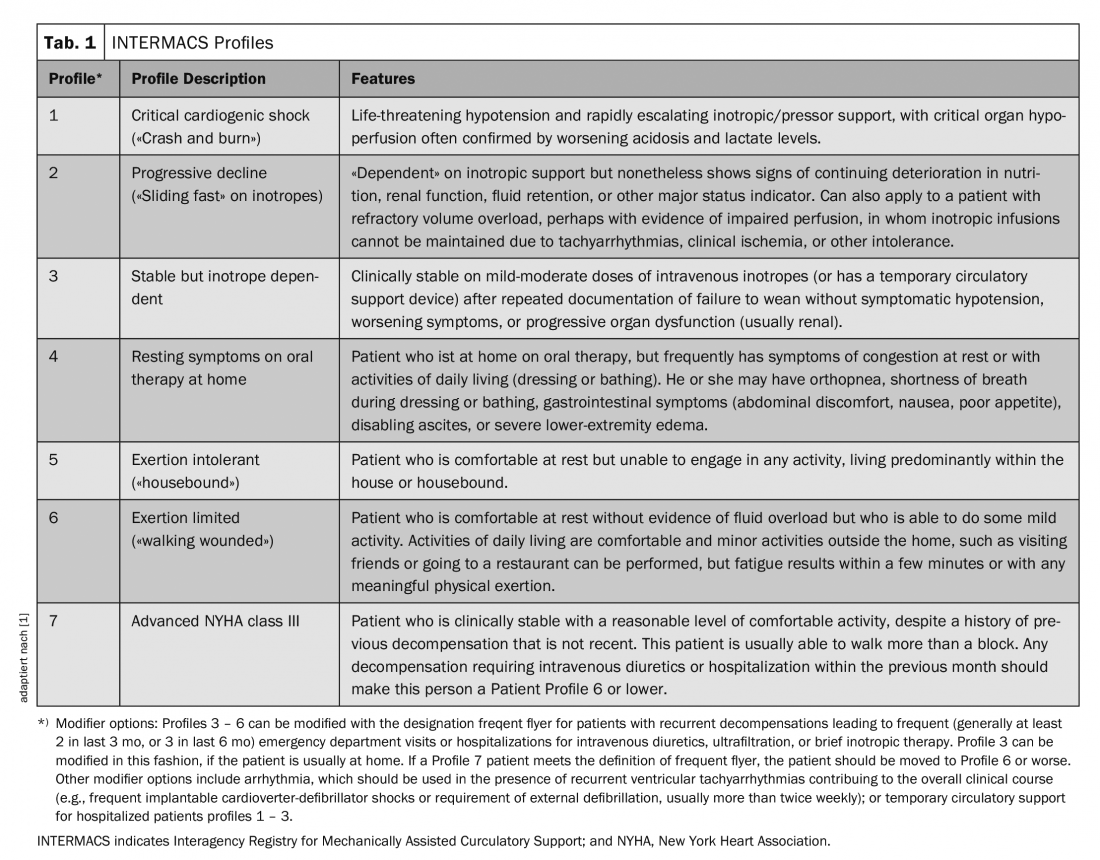
Das grösste Register über Patienten mit mechanischen Unterstützungsdevices führt die internationale Gesellschaft für Herz- und Lungentransplantation (IMACS; International Society for Heart and Lung Transplantation Mechanical Circulatory Support Registry). Es beinhaltet Daten aus 35 Ländern sowie den grossen Registern aus Europa (EUROMACS), der USA (INTERMACS) und Japan (J-MACS) [2]. Zwischen Januar 2013 und Dezember 2016 wurden insgesamt 14’062 Device Implantationen registriert, davon 93% reine LVADs, 5% biventrikuläre Unterstützungssysteme und 2% «total artificial hearts», also komplette Kunstherzen. 83% der Patienten waren in der IM Kategorie 1–3, knapp 28% waren aktiv für eine Herztransplantation gelistet, 41% erhielten ein LVAD als endgültige Therapie (Destination-Therapy).
Die Ein- und Zweijahres-Überlebensrate lag bei Patienten nach LVAD Implantation mit kontinuierlichem Fluss bei 81% respektive 71%. Patienten mit IM Profil 1 hatten eine deutlich schlechtere Einjahres-Überlebensrate als solche mit IM 3 (71% vs. 84%), die beste Zwei- und Dreijahres-Überlebensrate zeigte sich bei Patienten mit IM Profil 5–7, also bei ambulanten Patienten mit schwerer Herzinsuffizienz.
Warten wir zu lange?
Die ROADMAP Studie ging dieser Fragestellung nach und schloss 200 ambulante Patienten mit schwerer Herzinsuffizienz (IM Profil ≥4, Gehstrecke im 6 min Gehtest (6 MWT) <300 Meter, mindestens eine Hospitalisation oder zwei Vorstellungen auf der Notfallstation aufgrund von Herzinsuffizienz im letzten Jahr), die nicht für eine Herztransplantation qualifizieren, in diese prospektive, nicht randomisierte multizentrische Studie ein [3]. Die Patienten konnten sich gemeinsam mit ihren Ärzten für eine optimale medikamentöse Therapie (OMT) oder eine LVAD Implantation (Destination-Therapy) entscheiden. Der primäre Endpunkt war Überleben unter der ursprünglich gewählten Therapie sowie einer Verbesserung von 75 Meter oder mehr im 6 MWT. Sekundäre Endpunkte waren unter anderem die Erhebung der Lebensqualität (EuroQol 5 dimensions, 5-level questionnaire, EQ-5D-5L) sowie eines Depression Scores (Patient Health Questionnaire, PHQ-9) mittels Fragebogen, der NYHA Klasse und der unerwünschten Ereignisse.
Wie zu erwarten, waren die Patienten, die sich initial für ein LVAD entschieden insgesamt kränker und hatten eine schlechtere Lebensqualität (LVAD Gruppe vs. OMT Gruppe: Lebensqualität (EQ-5D VAS) 44 vs. 66 Punkte, Depressionen (PHQ-9 Score) 10 vs. 7 Punkte, NYHA IV 52% vs. 25%, Intermacs Profil 4 65% vs. 34%, IM 5 oder höher 32% vs. 64%).
Trotz der ungünstigeren Ausgangslage zeigten mehr Patienten zwei Jahre nach LVAD Implantation eine Verbesserung der Leistungsfähigkeit auf eine NYHA Klasse I/II (69% vs. 37% unter OMT) und die Gehstrecke nahm signifikant zu. Des Weiteren gaben die Patienten eine signifikante Verbesserung der Lebensqualität (EQ-5D VAS +27Pkt) sowie der Stimmungslage (Depression Scores PHQ 9 Score –4,6Pkt) an. In der Gruppe der OMT konnte keine signifikante Veränderung detektiert werden.
Interessant ist jedoch, dass sich innerhalb der nächsten zwei Jahre fast ein Viertel der Patienten in der OMT-Gruppe (21%) für eine LVAD Implantation entschied, und dies im Median bereits 4,9 Monate nach Einschluss. Mehr als die Hälfte der Patienten (55%) mit verzögerter LVAD-Implantation waren zu diesem Zeitpunkt bereits unter Therapie mit Inotropika, 70% hatten eine NYHA-Stadium IV erreicht und die mediane Gehstrecke verminderte sich von initial 219 m auf 90 m.
Rechnet man diese relativ grosse Gruppe an Patienten mit verspäteter LVAD Implantation zu der OMT-Gruppe (intention-to-treat), so zeigt sich zwischen beiden Gruppen kein signifikanter Unterschied im Überleben. Trennt man sie jedoch nach der tatsächlich erhaltenen Therapie auf, so sieht man, dass nur 41% der OMT Gruppe, aber 70% der LVAD Gruppe unter der ursprünglichen Therapie überlebten.
Die Anzahl an unerwünschten Nebenwirkungen (AEs) war in der LVAD-Gruppe höher als in der OMT-Gruppe. Die häufigsten AEs nach LVAD-Implantation waren Blutungen, Driveline-Infektionen, Pumpenthrombosen und Schlaganfälle; in der OMT-Gruppe vor allem die Verschlechterung der Herzinsuffizienz (50% der Patienten). Überraschenderweise gaben die Patienten mit LVAD trotz der AEs und häufigeren Hospitalisationen (86% vs. 78%) eine bessere Lebensqualität und Stimmungslage an.
Teilt man die Patienten nach dem Schweregrad ihrer Erkrankung auf, so sieht man, dass vor allem die Patienten mit IM 4 profitierten, jene mit IM 5–7 nur dann, wenn sie zuvor eine eingeschränkte Lebensqualität angegeben haben.
Fasst man alle Erkenntnisse dieser Studie zusammen, so kann man sagen, dass bei Patienten mit IM 5–7 die eine akzeptable Lebensqualität angeben, mit einer Implantation zugewartet werden kann ohne eine exzessive Mortalität zu riskieren, solange diese regelmässig und engmaschig an einem Zentrum kontrolliert werden (im Median trat die Verschlechterung in dieser Studie nach nur 4,9 Monaten auf).
Therapieoptimierung vor LVAD-Implantation
Seit der Durchführung der ROADMAP Studie und der letzten Datenerhebung des IMACS Registers 2016 sind neuere medikamentöse (Sacubitril-Valsartan) und interventionelle (MitraClip®, Vorhofflimmerablation) Therapien in der täglichen Praxis vermehrt zur Anwendung gekommen. Im PARADIGM-HF Trial zeigte sich unter der Therapie mit Sacubitril-Valsartan bei weniger kranken Patienten (nur weniger als 1% hatten NYHA IV, der Grossteil ca. 70% NYHA II) eine relative Reduktion der Mortalität sowie der Hospitalisationen aufgrund von Herzinsuffizienz um je 20% im Vergleich zur Therapie mit Enalapril [4]. In CASTLE-AF fand sich, in einer sehr selektionierten Patientengruppe mit Herzinsuffizienz und Vorhofflimmern, eine relative Reduktion des kombinierten Endpunktes von Tod und Rehospitalisation aufgrund von Herzinsuffizienz um 38% nach Vorhofflimmerablation [5]. Der COAPT Trial zeigte eine Reduktion der Mortalität (RRR –38%) und der Rehospitalisationsrate aufgrund von HI (RRR –47%) nach MitraClip® Implantation im Vergleich zur medikamentösen Therapie bei Patienten mit schwere sekundärer Mitralinsuffizienz und Herzinsuffizienz [6]. Auch wenn sicher nicht alle Patienten von diesen Therapien profitieren, so stehen uns mehr und mehr Möglichkeiten zur Verfügung, um diesen schwer kranken Patienten zu helfen.
Doch auch auf technischer Seite haben sich in den letzten Jahren viele Entwicklungen gezeigt, die die Komplikationsrate nach LVAD Implantation senken konnten. Einerseits ermöglichen neuere Daten ein optimaleres Management der Patienten (so konnte im ENDURANCE Supplemental Trial eine deutliche Reduktion der Schlaganfall-Rate durch eine bessere Blutdruckeinstellung erreicht werden), anderseits haben sich mit der neusten Generation des LVAD (HeartMate 3®, Abbott) auch technische Veränderungen gezeigt [7]. In der MOMENTUM 3 Studie fand sich nach Implantation des HeartMate 3®(einer Zentrifugalpumpe) insgesamt eine signifikant verminderte Rate an Schlaganfällen (10% vs. 19%, wobei die Anzahl schwerer Schlaganfälle (modified Rankin score of >3) gleichblieb), sowie eine deutlich tiefere Rate möglicher oder bestätigter Pumpenthrombosen (1,1% vs. 15,7%) im Vergleich mit dem HeartMate 2®. Kein einziges HeartMate 3® musste aufgrund des Verdachts auf eine Pumpenthrombose ersetzt oder explantiert werden, hingegen war dies bei 12% der Patienten mit HeartMate 2® der Fall [8].
Für jeden Patienten die optimierte Therapie
Mit all den technischen, interventionellen und medikamentösen Möglichkeiten können wir Patienten mit Herzinsuffizienz heute viel mehr Optionen anbieten als früher. Gleichzeitig bringt das auch die Verpflichtung mit sich, für jeden Patienten die für ihn/sie geeignete Therapie zu finden. Um dem Patienten und seinen Angehörigen die Möglichkeit zu geben, sich mit allen gegebenen Vor- und Nachteilen jeder Therapie in Ruhe auseinandersetzten zu können und Eingriffe, so gewollt, in einem elektiven Rahmen durch zu führen, ist es wichtig, die Patienten frühzeitig an einem Zentrum für schwere Herzinsuffizienz kennen zu lernen und die weitere Betreuung gemeinsam mit den behandelnden Hausärzten, Kardiologen sowie weiteren involvierten Personen im Umfeld zu koordinieren.
Für die Identifikation der Patienten, die eine weiterführende Evaluation an einem Zentrum benötigen ist die Merkhilfe «I need help» sehr hilfreich (Tab. 2). Insbesondere Patienten mit rezidivierenden kardialen Dekompensationen oder jenen, bei denen es unmöglich ist die Herzinsuffizienzmedikation zu steigern oder diese sogar reduziert werden muss, sollten einem Spezialisten zur Abklärung zugewiesen werden.
Der letztendliche Entscheid für oder gegen ein LVAD muss vor allem mit Rücksicht auf die Wünsche und Lebensvorstellungen des Patienten, unter Einbezug seines sozialen Netzwerkes (Freunde, Angehörige) gemeinsam mit dem Patienten, seiner Familie und den Caregivern (z.B. dem Hausarzt, Kardiologen, Spitex) getroffen werden (Abb. 1).
Take-Home-Messages
- Für Patienten mit Herzinsuffizienz stehen uns heute immer mehr medikamentöse (Sacubitril-Valsartan), interventionelle (CRT, Mitralclip® bei Mitralinsuffizienz, Ablation bei Vorhofflimmern) und technische (LVAD) Therapien zur Verfügung. Um Patienten, Angehörigen sowie den behandelnden Ärzten die Möglichkeit zu geben, alle zur Verfügung stehenden Therapieoptionen in Ruhe zu besprechen und die optimale Behandlung für jeden einzelnen Patienten zu finden, ist es wichtig, diese möglichst früh an einem Zentrum für Herzinsuffizienz vorzustellen.
- Als Orientierungshilfe, wann Patienten spätestens zu einem HI-Spezialisten geschickt werden sollen, bietet sich die Merkhilfe «I need help» an.
- In den letzten Jahren konnte durch ein besseres Patientenmanagement sowie durch technische Fortschritte eine Reduktion der schwerwiegenden Komplikationen (z.B. Pumpenthrombosen, Schlaganfall) für Patienten mit LVAD erreicht werden. Aufgrund des gleichzeitig steigenden Mangels an Spenderorganen stellt die LVAD Implantation daher für immer mehr Patienten mit schwerer Herzinsuffizienz eine gute Alternative dar.
- Bei Patienten mit INTERMACS Profil 5–7 sowie erhaltener Lebensqualität sollte mit einer LVAD Implantation zugewartet werden. Eine engmaschige Kontrolle ist unabdingbar, um die ersten Zeichen einer oft raschen Verschlechterung nicht zu übersehen und somit riskante Hochrisikoeingriff zu verhindern.
- Patienten mit INTERMACS Profil 5–7 mit einer eingeschränkten Lebensqualität müssen abwägen, ob sie für die Chance auf eine Verbesserung der Lebensqualität bereit sind, eine erhöhte Rate an Komplikationen in Kauf zu nehmen.
Literatur:
- Yancy CW et al.: 2013 ACCF/AHA guideline for the management of heart failure: a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. (Adapted from Stevenson et al. INTERMACS profiles of advanced heart failure: the current picture. J Heart Lung Transplant. 2009;28:535–4). Circulation 2013;128(16):e240-327.
- Kirklin JK, et al.: J Heart Lung Transplant 2018; 37(6): 685–691.
- Starling RC, et al.: Risk Assessment and Comparative Effectiveness of Left Ventricular Assist Device and Medical Management in Ambulatory Heart Failure Patients: The ROADMAP Study 2-Year Results. JACC Heart Fail 2017; 5(7): 518–527.
- McMurray JJ, et al.: Angiotensin-neprilysin inhibition versus enalapril in heart failure. N Engl J Med 2014; 371(11): 993–1004.
- Marrouche NF, et al.: Catheter Ablation for Atrial Fibrillation with Heart Failure. N Engl J Med 2018; 378(5): 417–427.
- Stone GW, et al.: Transcatheter Mitral-Valve Repair in Patients with Heart Failure. N Engl J Med 2018; 379(24): 2307–2318.
- Milano CA, et al.: HVAD: The ENDURANCE Supplemental Trial. JACC Heart Fail 2018; 6(9): 792–802.
- Mehra MR, et al.: Two-Year Outcomes with a Magnetically Levitated Cardiac Pump in Heart Failure. N Engl J Med 2018; 378(15): 1386–1395.
- Baumwol J: «I Need Help»-A mnemonic to aid timely referral in advanced heart failure. J Heart Lung Transplant 2017; 36(5): 593–594.
CARDIOVASC 2019; 18(1): 16–19
Autoren
- Dr. med. Monika Wieser
- Dr. med. Daniel Rhyner
- Dr. med. Olivier Wigger
- Dr. med. Stephan Dobner
- Prof. Dr. med. Lukas Hunziker
Publikation
- CARDIOVASC



Comments are closed.