Zu den häufigsten Ursachen für eine chronische Nierenerkrankung (CKD) zählen Diabetes und Hypertonie. Bei erhöhtem CKD-Risiko wird ein regelmässiges Screening empfohlen. Neben der eGFR sollte auch die Albuminurie bestimmt werden. Um Auftreten und Fortschreiten einer CKD im Rahmen eines multimodalen Behandlungskonzepts entgegenzuwirken, stehen heutzutage neben der RAAS-Inhibition auch innovative Wirkstoffe wie SGLT-i und Finerenon zur Verfügung.
In der Schweiz und in Deutschland ist jeder zehnte Erwachsene von CKD (Chronic kidney disease, CKD) betroffen, wobei es eine hohe Dunkelziffer gibt [1,2,9]. Die chronische Nierenschädigung hat verschiedene mögliche Ursachen und kann eine Vielzahl an kardiovaskulären Veränderungen nach sich ziehen. CKD beschleunige Entwicklung und Fortschreiten von Arteriosklerose und Atherosklerose, berichtete Dr. med. Frederic Bauer, Chefarzt der Klinik für Nephrologie und Dialyse im Elisabeth-Krankenhaus Essen (D). Während Atherosklerose eine Erkrankung der Intima beschreibt, betrifft die Arteriosklerose Typ Mönckeberg vor allem die Media. «Die chronische Niereninsuffizienz ist ein eigenständiger und wichtiger kardiovaskulärer Risikofaktor», betonte der Referent [1,3]. Dies habe zur Folge, dass viele CKD-Patienten aufgrund von kardiovaskulären Ereignissen versterben. «Wir wollen das deutlich erhöhte kardiovaskuläre Risiko senken, indem wir an allen Stellschrauben drehen und Voraussetzung dafür ist, dass wir die Diagnose frühzeitig stellen», so der Referent. Da die CKD oft asymptomatisch ist, ist sie erheblich unterdiagnostiziert. Personen mit einem hohen Risiko sollten daher gescreent werden [2].
Erhöhte Albuminurie gilt auch bei normaler eGFR als Risikofaktor
Gemäss KDIGO (Kidney Disease: Improving Global Outcomes) wird CKD definiert durch eine >3 Monate bestehende strukturelle oder funktionelle Störung der Niere mit Implikationen, die gesundheitsrelevant sind. Klassifiziert wird die CKD nach dem «CGA»-Schema: Ursache (Cause, C), glomeruläre Filtrationsrate (GFR, G) und Albuminurie (A). Die CGA-Stadieneinteilung der CKD nach KDIGO ist in Tabelle 1 ersichtlich. Dr. Bauer hob hervor, dass sowohl eine erniedrigte eGFR, als auch Albuminurie (UACR ≥30 mg/g) relevant seien für eine chronische Niereninsuffizienz [1]. «Beides sind wichtige und unabhängige Prädiktoren der Gesamtmortalität», betonte der Referent. Für die Albuminurie (Albumin-Kreatinin-Ratio im Urin, UACR) wird nicht 24h-Sammelurin benötigt, sondern Spontanurin sei ausreichend [1].
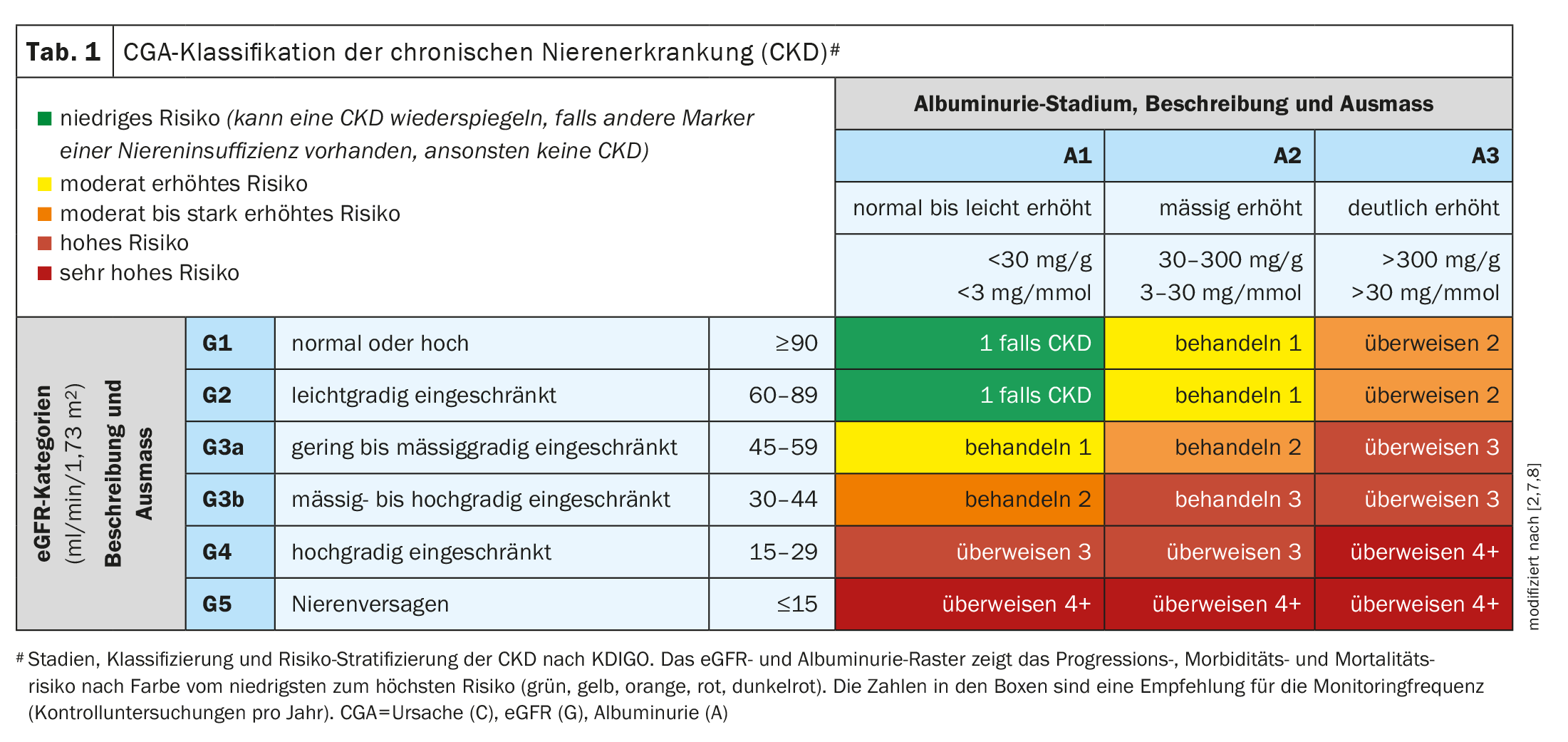
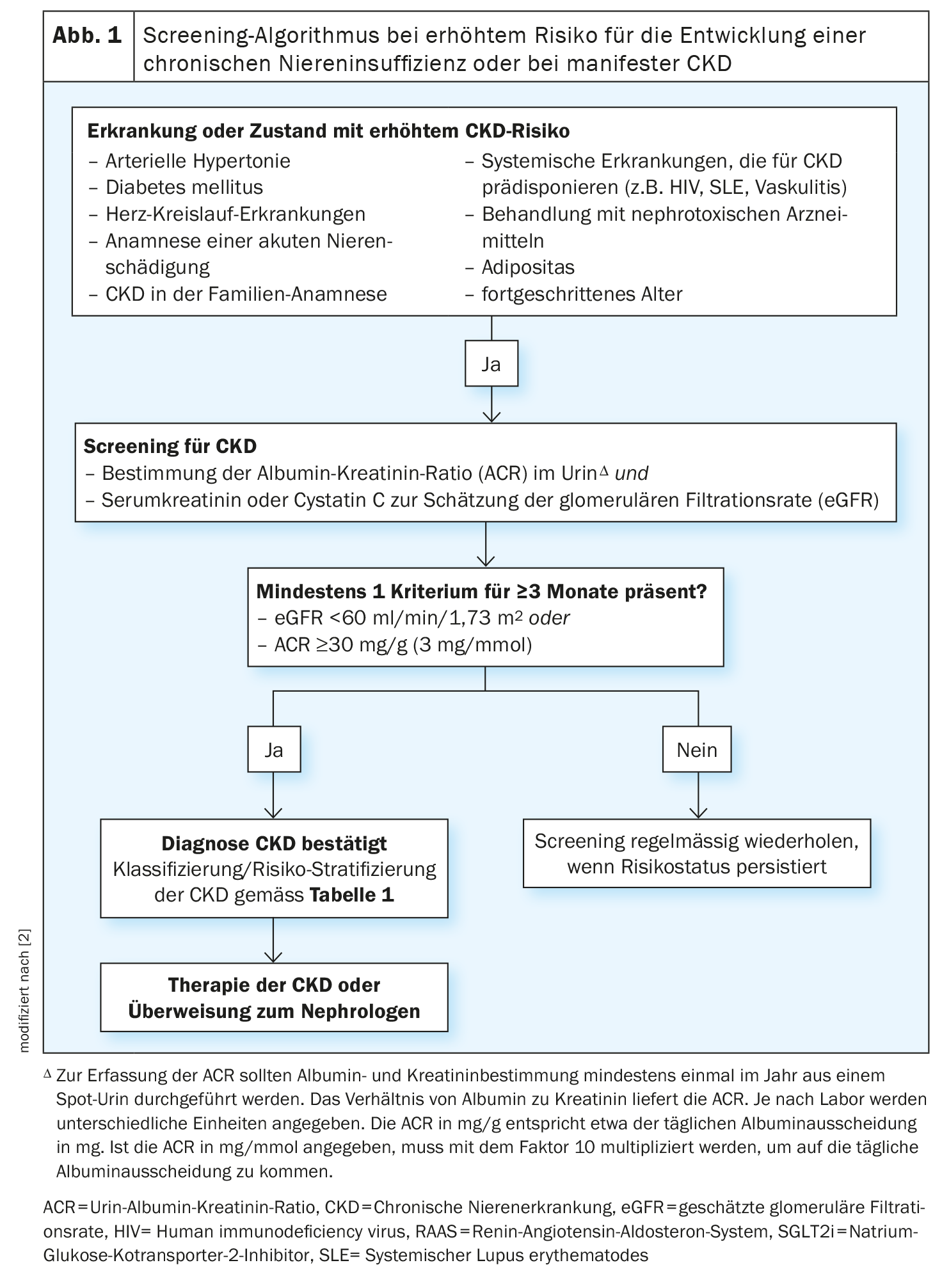
Bereits ab einer eGFR <60 ml/min/1,73 m2 steigen kardiovaskuläre Risiken, Hospitalisierungsraten und Mortalität stark an, so Dr. med. Alexander Beck, Facharzt für Innere Medizin und Kardiologie in Essen (D) [1]. In den Richtlinien zu Screening und Identifikation einer CKD der Schweizerischen Gesellschaft für Nephrologie wird daher empfohlen, Patienten mit arterieller Hypertonie, Diabetes mellitus und Herz-Kreislauf-Erkrankungen mindestens einmal jährlich auf das Vorliegen einer CKD zu testen (eGFR und UACR) [2]. Dr. Beck riet, auch Patienten mit positiver Familienanamnese bezüglich CKD oder einer in der Vorgeschichte dokumentierten deutlichen Verschlechterung der Nierenfunktion hin und wieder zu screenen [1]. «Wenn wir diese Patienten früh erkennen und früh behandeln, senken wir nicht nur das Dialyserisiko, sondern auch das kardiovaskuläre Risiko», betonte der Referent [1]. Die CKD-Stadien 3–4 machen fast die Hälfte aller CKD-Patienten aus. Daraus ergebe sich ein grosses Potenzial, Prävention zu betreiben und kardiovaskuläre Ereignisse zu verhindern, so Dr. Beck [1]. Bei der eGFR gebe es individuelle Schwankungen, die UACR sei eigentlich der stabilere Parameter. Wenn es Auffälligkeiten gibt beim CKD-Screening, sind sonografisch strukturelle Veränderungen der Niere auszuschliessen. Patienten mit hohem und sehr hohem Risiko sollten an den Nephrologen überwiesen werden (Abb. 1)[1].
Progressionshemmung mit RAAS-Inhibition, SGLT-2-i und Finerenon
Im zweiten Teil des Symposiums erläuterte Dr. Bauer einen multimodalen Ansatz, um die Progredienz einer Niereninsuffizienz zu bremsen [1]. Hinsichtlich Lebensstilmodifikation decken sich die Empfehlungen für Patienten mit hoher Proteinurie und erniedrigter eGFR weitgehend mit denjenigen für Hypertoniker und Diabetiker: Gewichtskontrolle, Blutdruckinstellung, Bewegung, Salzreduktion, Rauchstopp [1]. Auch sollten nephrotoxische Medikamente (z.B. nicht- steroidale Antirheumatika, NSAR) nach Möglichkeit vermieden werden. Neben der bewährten Behandlung von Bluthochdruck und Senkung der Albuminurie mit Renin-Angiotensin-System-(RAAS)-Inhibitoren wie Angiotensin-Converting-Enzym-(ACE)-Inhibitoren oder Angiotensin-II-Rezeptor-Blockern (ARB), gibt es heute mit SGLT-2-Inhibitioren und Finerenon zwei weitere progressionshemmende Substanzklassen. «Die RAAS-Inhibition ist der Klassiker der nephroprotektiven Therapie, vor allem für Patienten mit Albuminurie», so der Referent [1]. Der Druck im Glomerulus wird reduziert und damit verringert sich die Hyperfiltration. Fast alle CKD-Patienten weisen eine weisen eine glomeruläre Hyperfiltration auf auf, welche auf lange Sicht die Filtereinheiten der Niere schädigen. Man sollte die Patienten darüber aufklären, dass unter der RAAS-Inhibition das Kreatinin sich etwas verschlechtern könne. Durch eine maximale RAAS-Inhibition lasse sich die Mortalität senken, gegebenenfalls solle man einen Nephrologen beiziehen, so Dr. Bauer.
Dass die SGLT-2-Inhibtion mit Dapagliflozin zusätzlich zur RAAS-Blockade sowohl bei CKD-Patienten mit als auch ohne Diabetes zu einer signifikanten Reduktion renaler Endpunkte führt, konnte unter anderem in der DAPA-CKD-Studie eindrücklich gezeigt werden [4]. Neben Forxiga® sind in der Schweiz für Diabetiker auch Fixkombinationen von Dapagliflozin mit Metformin und/oder Saxagliptin zugelassen. Neben Dapagliflozin ist mittlerweile auch Empagliflozin zugelassen, das in der EMPA-Kidney-Studie nephroprotektive Effekte bewies [5]. Neben Jardiance® stehen auch Fixkombinationen mit Metformin und oder Linagliptin zur Verfügung.
SGLT-2 ist ein Carrier-Protein, welches im proximalen Tubulus der Niere ungefähr 90% der filtrierten Glucose rückresorbiert. Wird dies durch die SGLT-2-Inhibitoren reduziert, erhöht sich die Natrium-Konzentration an der Macula densa und über das tubulo-glomeruläre Feedback kommt es zu einer Konstriktion der afferenten Arteriolen am Glomerulus und somit auch zu einer Reduktion der glomerulären Hyperfiltration. Bei akuter Erkrankung sollten SGLT-2-Inhibitoren abgesetzt werden aufgrund eines etwas erhöhten Ketoazidoserisikos.
Für Patienten mit CKD und Diabetes steht zudem auch Finerenon (Kerendia®) zur Verfügung. Finerenon ist ein Wirkstoff aus der Gruppe der Aldosteron-Antagonisten. Die Effekte beruhen auf dem selektiven Antagonismus an Mineralcorticoid-Rezeptoren. Finerenon bewies in den Studie FIDELIO-CKD bzw. FIGARO-CKD nephroprotektive bzw. kardioprotektive Effekte bei Diabetikern [6]. Für CKD-Patienten ohne Diabetes laufen die Studien aktuell noch [1].
Kongress: FomF Allgemeinmedizin Refresher
Literatur:
- «CKD – Screening, frühe Diagnose und moderne Therapie – Nephround- Kardioprotektion in der hausärztlichen Praxis», Symposium, AstraZeneca GmbH, FOMF Allgemeinmedizin Refresher Köln, 17.–20.01.2024.
- Schweizerische Gesellschaft für Nephrologie, Richtlinien zu Screening und Identifikation der Chronischen Niereninsuffizienz für Allgemeinmediziner und Internisten, www.swissnephrology.ch/wp/wp-content/
uploads/2023/01/161121_SGN_Pocketguide_CKD_Web_A4_d_WZ.pdf, (letzter Abruf 26.01.2024) - Gansevoort RT, et al.: Chronic kidney disease and cardiovascular risk: epidemiology, mechanisms, and prevention. Lancet 2013; 382: 339–352.
- Heerspink HJL, et al.; DAPA-CKD Trial Committees and Investigators. Dapagliflozin in Patients with Chronic Kidney Disease. NEJM 2020; 383(15): 1436–1446.
- The EMPA-KIDNEY Collaborative Group; Herrington WG, et al.: Empagliflozin in Patients with Chronic Kidney Disease. NEJM 2023; 388(2): 117–127.
- Agarwal R, et al.: FIDELIO-DKD and FIGARO-DKD Investigators. Investigating new treatment opportunities for patients with chronic kidney disease in type 2 diabetes: the role of finerenone. Nephrol Dial Transplant 2020.
- Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. Kidney Int 2013; 3(Suppl): 1–150.
- American Diabetes Association. Diabetes Care 2021 Jan; 44: 10.2337/dc21-S005
- Ogna VF, et al.: Prevalence and determinants of chronic kidney disease in the Swiss population. Swiss Med Wkl 2016;146: w14313.
HAUSARZT PRAXIS 2024; 19(2): 26–27 (veröffentlicht am 18.2.24, ahead of print)
Autoren
- Mirjam Peter, M.Sc.
Publikation
- HAUSARZT PRAXIS




Comments are closed.