Für Patienten mit axialer Spondyloarthritis (axSpA), bei welchen eine Therapie mit nichtsteroidalen Antirheumatika nicht zielführend war, stehen heutzutage mehrere Wirkstoffe aus den Substanzklassen der Biologika und der JAK-Inhibitoren zur Verfügung. Ein wichtiges Auswahlkriterium ist neben der Wirksamkeit auch das Sicherheitsprofil des DMARD. Ausserdem sollten die Präferenzen des Patienten berücksichtigt werden. Die ASAS-EULAR Empfehlungen bieten auch eine Orientierung zum Vorgehen bei einer Therapieumstellung.
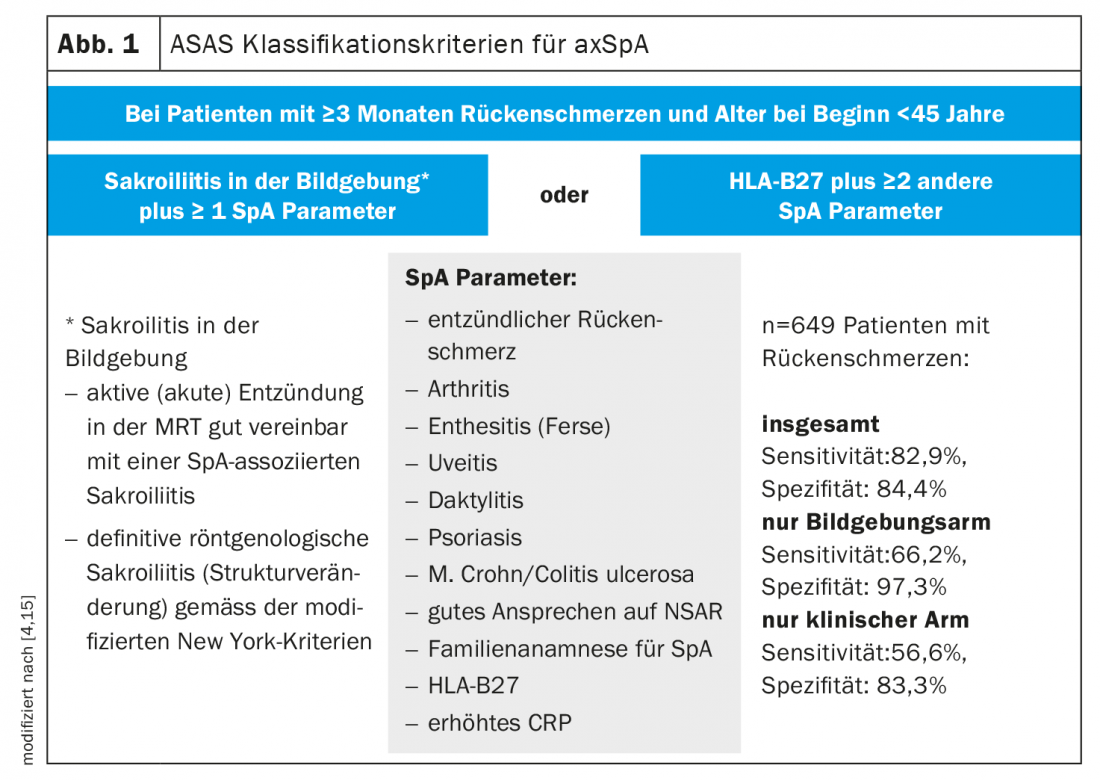
Anlässlich des diesjährigen EULAR Annual Meetings diskutierten namhafte Experten die aktuellsten Erkenntnisse zu Diagnose und Therapie der axialen Spondyloarthritis (axSpA). Unter einer axSpA versteht man eine entzündliche Wirbelsäulenerkrankung aus dem rheumatischen Formenkreis, die mit verschiedenen muskuloskelettalen und extraskelettalen Manifestationen einhergehen kann [1]. Das Kardinalsymptom der axSpA ist entzündlicher Rückenschmerz. Die diagnostische Abklärung beinhaltet Röntgen- und MRT-Untersuchung der Lendenwirbelsäule (LWS) und der Iliosakralgelenke sowie ein Laborscreening, das inflammatorische Marker (BSG, CRP) und Testung auf HLA-B27 umfasst [2]. Die Anamnese sollte neben extraartikulären Manifestationen auch die Exploration psychsozialer Belastungen/arbeitsbezogener Belastungen beinhalten. Zur Diagnosesicherung wurden die ASAS («Assessment of SpondyloArthritis International Society»)-Klassifikationskriterien etabliert (Abb. 1) [3]. Diese verlangen zwingend einen Nachweis von HLA-B27, ein weiteres Kriterium ist mittels Bildgebung feststellbare Sakroiliitis. Bei denjenigen Patienten ohne strukturelle Veränderungen spricht man von nicht-röntgenologischer axialer SpA, während Patienten mit strukturellen Veränderungen in den Iliosakralgelenken der ankylosierenden Spondyloarthritis (Morbus Bechterew) zugeordnet werden. Zur Erfassung der Krankheitsaktivität stehen neben Ergebnissen der klinischen Untersuchung, der Bildgebung und der Labordiagnostik neben dem BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) auch der neuere ASDAS (Ankylosing Spondylitis Disease Activity Score) zur Verfügung, der auf einigen BASDAI-Fragen beruht und das CRP einschliesst [4–7]. Die Krankheitsaktivität soll in regelmässigen Abständen – zumeist alle 3 bis 6 Monate – mit Hilfe der klinischen Composite-Scores überprüft werden [3,5].
Multimodales Behandlungskonzept
Zur Behandlung von Patienten mit axSpA wird eine Kombination aus nicht-pharmakologischen Massnahmen (z.B. Bewegungstherapie) und medikamentöser Therapie empfohlen [1]. Neben Schmerzreduktion wird der Erhalt der körperlichen Funktionsfähigkeit und die Verhinderung struktureller Läsionen angestrebt [5,8,9]. Die Ziele der medikamentösen Behandlung sind in erster Linie eine Reduktion der Krankheitsaktivität und das Erreichen einer klinischen Remission. Dies schliesst Schmerzreduktion, eine Verringerung inflammatorischer Prozesse und eine Hemmung der röntgenologischen Progression ein. Nichtsteroidale Antirheumatika (NSAR) gelten bei axialer SpA nach wie vor als Erstlinientherapie [5]. Aufgrund des Sicherheitsprofils der NSAR-Präparate sollte die Dosierung und Dauer der Therapie fortwährend überprüft werden. Bei Patienten, die unter der Standardtherapie mit NSAR keine ausreichende Reduktion der entzündlichen Krankheitsaktivität erreichen, können Disease Modifying Anti-Rheumatic Drugs (DMARDs) eingesetzt werden.
Biologika und JAK-Inhibitoren – was ist der aktuelle Kenntnisstand?
Prof. Dr med. Désirée van der Heijde, Leiden University Medical Center (NL), gab einen aktuellen Überblick zu bDMARD und tsDMARD als Therapieoption bei axSpA [10]. Eine der Neuerungen in den 2022 aufdatierten ASAS-EULAR Empfehlungen für das Management von axSpA sei, dass vorrangig die ASDAS-Kriterien (Abb. 1) verwendet werden zur Beurteilung des Krankheitsverlaufes, die BASDAI-Kriterien haben an Bedeutung verloren. Wenn trotz NSAR-Therapie eine anhaltend hohe Krankheitsaktivität vorliegt mit einem ASDAS-Score ≥2,1 wird vorgeschlagen, eine Therapie mit einem TNFα-Inhibitor (TNFα-i), IL-17-Inhibitor (IL-17-i) oder Januskinase-Inhibitor (JAK-i) zu beginnen. Obschon die Wirksamkeitsdaten für Biologika und JAK-i ähnlich sind, wird im Allgemeinen dazu geraten, zunächst einen Therapieversuch mit TNFα-i oder IL-17-i zu starten. «Für die Präferenz von TNFα-Hemmern und IL-17-Inhibitoren gegenüber JAK-Inhibitoren sind vorwiegend Sicherheitsaspekte ausschlaggebend», erklärt die Referentin.
Hinsichtlich dem IL-17-i Secukinumab zeigen Daten aus der Verlängerungsphase randomisiert-kontrollierter Studien eine geringe Rate an schwerwiegenden Infektionen, Malignitäten und kardiovaskulären Ereignissen. Bezüglich Ixekizumab, ebenfalls ein IL-17-i, ist die Datenlage gering. Dies gilt auch für JAK-i, hier liegen lediglich Daten aus Kurzzeit-RCTs vor.
Bei Patienten mit Rheumatoider Arthritis (RA) und bestimmten Risikofaktoren weisen Daten der Studie Oral Surveillance darauf hin, dass JAK-i mit einem erhöhten Risiko für kardiovaskuläre Ereignisse (MACE) und Malignitäten assoziiert sind. Die Referentin betont, dass die RA-Patientenpopulation nicht gleichzusetzen sei mit der axSpA-Population [10,14]. Dennoch mahnt sie auch bei Patienten mit axialer SpA und bestimmten Risikofaktoren in Anbetracht der geringen Datenlage bezüglich JAK-i zur Vorsicht. Jedenfalls gelte es Nutzen und Risiken im Einzelfall sorgfältig abzuwägen.
In Tabelle 1 ist die Wirksamkeit von bDMARDs und tsDMARDs auf verschiedene Manifestationen der axSpA zusammengefasst. Beobachtungsstudien weisen darauf hin, dass Adalimumab, Infliximab, Golimumab und Certolizumab pegol eine höhere Wirksamkeit aufweisen bezüglich Uveitis als Secukinumab und Etanercept [11]. Hinsichtlich der JAK-Inhibitoren Tofacitinib und Upadacitinib hierzu liegen keine Daten vor.

Behandlungsversuch mit einem DMARD gescheitert – wie weiter?
Zur Frage, was man unternehmen kann, wenn die Behandlung mit einem bDMARD nicht zielführend war, rät Prof. van der Heijde: «Dann sollte als Erstes die Diagnose überdacht werden». Dies gilt insbesondere dann, wenn Patienten mit Rückenschmerzen weder auf eine Therapie mit TNFα-i noch IL-17-i angesprochen haben. Liegt eine hohe Krankheitsaktivität vor, sollte man sich fragen, ob andere Komorbiditäten oder Patientenmerkmale gegeben sind, welche dies beeinflussen könnten. In solchen Fällen empfiehlt sich ein MRI, um festzustellen, ob in der Wirbelsäule Hinweise auf eine Entzündung vorliegen. Wie lautet die konkrete Empfehlung der aufdatierten ASAS-EULAR Empfehlungen hierzu? Diese besagt, dass nach einem ersten gescheiterten Behandlungsversuch mit bDMARD oder tsDMARD zu einem anderen bDMARD (TNFα-i oder IL-17-i) oder einem JAK-i gewechselt werden sollte. Insgesamt sei die Datenlage zur Therapieumstellung nach gescheitertem Behandlungsversuch mit einem oder mehreren bDMARD oder tsDMRAD zum jetzigen Zeitpunkt eher gering, so die Referentin. Zu Secukinumab gibt es Daten, die zeigen, dass bei Patienten, die einen gescheiterten Behandlungsversuch mit TNFα-i hinter sich haben, gute Ansprechraten erzielt werden, obschon die Responseraten bei Biologika-naiven Patienten tendenziell besser waren [12]. Dasselbe Pattern zeigte sich in entsprechenden Studien zu Ixekizumab [13].
Wichtig für die Behandlung von Patienten mit axSpA sei auch stets, die übergordneten allgemeinen Therapieprinzipien zu berücksichtigen, betont die Referentin. Die Entscheidungsfindung für die bestmögliche Behandlungsoption sollte gemeinsam mit dem Patienten erfolgen («Shared decision making»). Dabei gilt es auch individuelle und soziale Kriterien miteinzubeziehen. Gegebenenfalls kann neben Wirksamkeit, Sicherheit und Kostenfaktor auch die Applikationsform (sc, iv, oral) ein Kriterium für die Auswahl der jeweils am besten passenden Behandlung sein.
Kongress: EULAR Annual Meeting
Literatur:
- Kiltz U, et al.: Langfassung zur S3-Leitlinie Axiale Spondyloarthritis inklusive Morbus Bechterew und Frühformen, Update, Z Rheumatol 2019(78): 3–64.
- Rudwaleit M: Spondyloarthritiden. Z Rheumatol 2017; 76(10): 889–903.
- Holak G: Diagnose und Therapie der axialen Spondyloarthritis. DFP-Literaturstudium 2021, www.pains.at/wp-content/uploads/SN-1-21-DFP-Diagnose-und-Therapie-der-axialen-Spondyloarthritis_komprimiert.pdf, (letzter Abruf 14.07.2022)
- Rudwaleit M, et al.: The early disease stage in axial spondylarthritis: results from the German Spondyloarthritis Inception Cohort. Arthritis Rheum 2009; 60(3): 717–727.
- Axiale Spondyloarthritis inklusive Morbus Bechterew und Frühformen, AWMF-Leitlinien Register Nummer: 060/003, Entwicklungsstufe: S3 Version: 2019.
- Garrett S, et al.: A new approach to defining disease status in ankylosing spondylitis: the Bath Ankylosing Spondylitis Disease Activity Index. J Rheumatol 1994; 21(12): 2286–2291.
- van der Heijde D, et al: ASDAS, a highly discriminatory ASAS-endorsed disease activity score in patients with ankylosing spondylitis. Ann Rheum Dis 2009; 68(12): 1811–1818.
- van der Heijde D, et al.: Preliminary core sets for endpoints in ankylosing spondylitis. Assessments in Ankylosing Spondylitis Working Group. J Rheumatol 1997; 24(11): 2225–2229; 321.
- van der Heijde D, et al.: Ankylosing spondylitis: plenary discussion and results of voting on selection of domains and some specific instruments. J Rheumatol 1999; 26(4): 1003–1005.
- «Targeted synthetic or biological DMARD in axial spondyloarthritis», Prof. Dr. med. Désirée van der Heijde, EULAR, 04.06.2022
- Lindström U, et al.: Anterior uveitis in patients with spondyloarthritis treated with secukinumab or tumour necrosis factor inhibitors in routine care: does the choice of biological therapy matter? Ann Rheum Dis 2021; 80(11): 1445–1452.
- Kivitz AJ, et al.: Efficacy and Safety of Secukinumab 150 mg with and Without Loading Regimen in Ankylosing Spondylitis: 104-week Results from MEASURE 4 Study. Rheumatol Ther 2018; 5(2): 447–462.
- Deodhar A: COAST-W Study Group. Efficacy and Safety of Ixekizumab in the Treatment of Radiographic Axial Spondyloarthritis: Sixteen-Week Results From a Phase III Randomized, Double-Blind, Placebo-Controlled Trial in Patients With Prior Inadequate Response to or Intolerance of Tumor Necrosis Factor Inhibitors. Arthritis Rheumatol 2019; 71(4): 599–611.
- Kragstrup TW, et al.: Waiting for JAK inhibitor safety data. RMD Open 2022 Feb; 8(1): e002236.
- Haller C: Axiale Spondyloarthritis, www.kssg.ch/system/files/media_document/2022-05/Axiale%20Spondyloarthritis.pdf, (letzter Abruf 14.07.2022).
HAUSARZT PRAXIS 2022; 17(8): 16–17
Autoren
- Mirjam Peter, M.Sc.
Publikation
- HAUSARZT PRAXIS




Comments are closed.