Psoriasis schlägt sich im Krankheitsverlauf häufig auch auf die Gelenke nieder – ungefähr ein Drittel der Betroffenen entwickelt im Laufe der Zeit eine Psoriasis-Arthritis (PsA). Die Verbesserung der Früherkennung und die Entwicklung präventiver therapeutischer Ansätze sind im Fokus verschiedener laufender Forschungsprojekte. Darunter sind beispielsweise Biomarker-Studien unter Anwendung von Omics-Technologien sowie Interventionsstudien zum zeitkritischen Einsatz verschiedener Biologika.
Die zentrale Frage laute, wie das Risiko für eine Psoriasis-Arthritis (PsA) mit Sicherheit vorhersagbar ist und ob PsA durch eine frühzeitige adäquate Intervention verhindert werden kann, erklärte Professor Laura Coates, Nuffield Department of Orthopaedics, Rheumatology and Musculoskeletal Sciences, University of Oxford (UK) [1]. Eine schlüssige Antwort auf diese Frage gibt es bislang nicht, aber zahlreiche Forschungsinitiativen bringen nach und nach Licht ins Dunkel. Bereits seit Längerem ist bekannt, dass rund 80% der Patienten eine Plaque-Psoriasis haben, bevor sie eine PsA entwickeln, sodass es sich bei der Hauptrisikogruppe um eine umschriebene Patientenpopulation handelt, die über Registerdaten und Krankenakten identifizierbar ist [2].
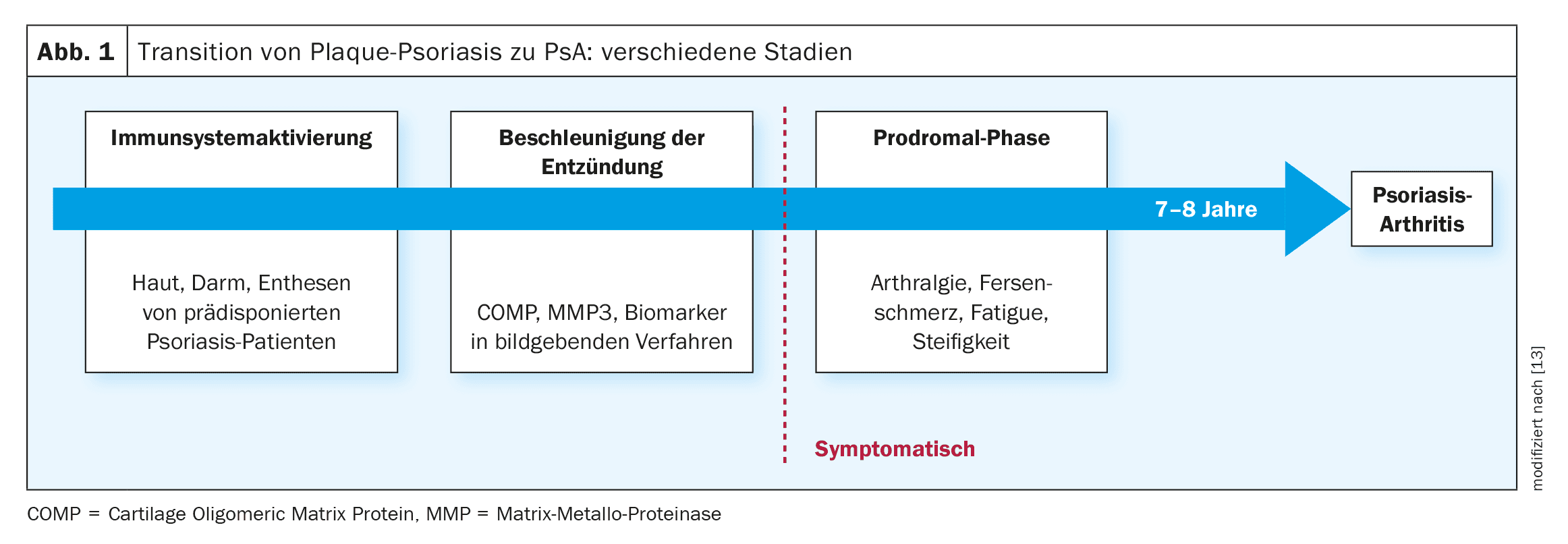
Prädiktoren für PsA: Risikomodelle und Self-Monitoring-Ansätze
Bisher gibt es zwar keine verlässlichen Verfahren oder Tests, die schnell, einfach und zuverlässig Hinweise auf die Entstehung einer PsA und ihren späteren Verlauf geben, aber mehrere Forschungsprojekte befassen sich mit diesem Themenkomplex. Forscher in Kanada haben ein Risikomodell entwickelt, anhand dessen basierend auf verschiedenen Patientenmerkmalen vorhergesagt werden kann, ob ein Psoriasis-Patient ein hohes Risiko hat, innert eines Zeitraums von 1 Jahr oder 5 Jahren eine PsA zu entwickeln [1,3]. Und am diesjährigen EULAR präsentierten britische Wissenschaftler Ergebnisse einer grossangelegten Sekundäranalyse basierend auf Daten aus dem UK CPRD (UK Clinical Practice Research Datalink), in welcher demografische Risikofaktoren für eine höhere Wahrscheinlichkeit, eine PsA zu entwickeln, ermittelt worden sind [4]. Zu diesem Zweck werteten die Forscher Falldaten von 122 330 Patienten mit Plaque-Psoriasis aus. Daraus ging hervor, dass sich bei 2460 der Betroffenen innert eines medianen Zeitraumes von 5,7 Jahren eine PsA manifestierte. Dabei wurden die folgenden demografischen Risikofaktoren identifiziert: Altersgruppe 30–50 Jahre, männliches Geschlecht, BMI >25.
Als Beispiele für «Digital Health»-Ansätze im Bereich Risikoabschätzung und frühzeitiger Diagnose von PsA nannte Prof. Coates das iPROLEPSIS-Projekt und die PSORCAST-Studie [1]. Im iPROLEPSIS-Projekt geht es um die Implementierung einer personalisierten digitalen Anwendung, welche zum einen Patienten auf spielerische Weise im «Disease Management» unterstützt und zum anderen zur Datenerfassung im Real-World-Setting beiträgt mit dem Ziel, neue Erkenntnisse zu gewinnen über wichtige Faktoren, welche bei Patienten mit bestehender Psoriasis die Entwicklung einer PsA begünstigen [5]. Die PSORCAST-Studie zielt darauf ab, eine Smartphone-App zu entwickeln und zu validieren, welche digitale, klinische und laborbezogene Daten integriert, um personalisierte PsA-Risikofaktoren zu eruieren und die frühzeitige PsA-Diagnose zu erleichtern [6]. Die Patienten können diese App im Alltag im Sinne von Self-Monitoring anwenden.
Lassen sich PsA-spezifische Biomarker identifizieren?
Im HIPPOCRATES-Konsortium sind Partnerinstitutionen aus Belgien, Dänemark, Deutschland, Irland, Italien, Spanien, Schweden, der Schweiz, den Niederlanden, Grossbritannien und den USA beteiligt [7]. Das Ziel besteht darin, neu entdeckte Marker und Verfahren, die der frühzeitigen Diagnose von PsA dienen könnten, in internationalen Patientenkohorten zu überprüfen. Darüber hinaus werden in dem HIPPOCRATES-Projekt personalisierte Behandlungsstrategien entwickelt, die das Ansprechen auf die Behandlung verbessern und die Entwicklung einer schweren Psoriasis-Arthritis hemmen sollen. Eine Grundidee besteht darin, durch die Identifikation molekularer PsA-Biomarker unter Patienten mit Plaque-Psoriasis eine frühzeitige Diagnose und Behandlung zu ermöglichen, sodass die Auswirkungen der Erkrankung abgemildert werden können. Zu diesem Zweck peilen Forscher mittels Anwendung von Multi-Omics-Technologie das Identifizieren einer molekularen Signatur an. In diesem Zusammenhang sei im Rahmen des HIPPOCRATES-Projektes eine Pilotstudie durchgeführt worden, berichtete die Referentin [1]. Dabei wurden Serumproben von 90 Personen, die am St. Vincent’s University Hospital in Dublin (Irland) an einer prospektiven Psoriasis-Studie (BioCOM) teilnahmen, mittels quantitativer Proteomik (LC-MS/MS-Analyse), gezielter Affinitätsproteomik, Metabolomik, Lipidomik und Genomik analysiert [1,8]. Von den 90 Teilnehmern hatten 30 eine etablierte PsA gemäss CASPAR-Kriterien, 30 eine Psoriasis ohne klinische muskuloskelettale Anzeichen und 30 hatten eine Psoriasis mit klinischen Symptomen, die auf eine frühe muskuloskelettale Beteiligung hindeuten. Die Forscher konnten molekulare Marker identifizieren, die eine Unterscheidung zwischen Psoriasis und PsA ermöglichen. In laufenden Studien werden die Multi-Omics-Daten integriert und einer Analyse durch maschinelles Lernen und KI unterzogen.
| PsA-Risikofaktoren |
| – Positive Familienanamnese |
| – Höherer Psoriasis-Schweregrad (PASI) |
| – Längere Dauer der Psoriasiserkrankung |
| – Arthralgien, Steifigkeit Fatigue |
| – Übergewicht (BMI >35) |
| – Uveitis in der Vorgeschichte |
| – Schilddrüsenerkrankung in der Vorgeschichte |
| – Spezifische Psoriasis-Lokalisation (Nagel, Kopfhaut, gluteal) |
| – Hyperlipidämie |
| – Depression |
| – Rauchen |
| – Trauma |
| nach [1,12] |
«Windows of opportunity» für Intervention mit Biologika?
In diesem Kontext liegt medikamentösen Interventionen mit Biologika die Hypothese zugrunde, dass bestimmte Wirksubstanzen durch antientzündliche Effekte sowohl die Hautsymptome als auch die Gelenkbeteiligung so beeinflussen können, dass die Progredienz aufgehalten wird. Dabei wird von einem zeitkritischen Einsatz der Biologika ausgegangen.
- Bei IVEPSA («Interception in Very Early PsA study») handelt es sich um eine offene prospektive explorative Studie, in welcher untersucht wurde, ob eine frühzeitige Intervention mit dem Interleukin(IL)-17A-Inhibitor Secukinumab zu einer umfassenden Remission der Hautsymptome, Schmerzen und subklinischen Entzündungen führt [9]. Einschlusskriterien waren Nagel- oder Kopfhautbefall oder ein PASI (Psoriasis Area Severity Index) >6, sowie entzündliche oder erosive Veränderungen im MRT oder CT. Die Patienten erhielten über 24 Wochen eine Behandlung mit Secukinumab. Klinische Bewertungen der Haut- und Gelenkerkrankungen wurden zu Studienbeginn sowie nach 12 und 24 Wochen durchgeführt. 20 Patienten wurden eingeschlossen, von denen 85% über Arthralgien berichteten und 40% bei der Untersuchung schmerzhafte Gelenke aufwiesen. 83% hatten mindestens eine entzündliche Läsion im MRT, die meisten von ihnen Synovitis/Enthesitis. Die Hauterkrankung (PASI: p<0,002; BSA: p<0,003) und die Arthralgie (VAS-Schmerz: p<0,003) verbesserten sich nach 24 Wochen deutlich. Der PSAMRIS (The psoriatic arthritis magnetic resonance imaging scoring system) und der Synovitis-Subscore verbesserten sich ebenfalls signifikant (p=0,005 bzw. p=0,008). Erosionen und Enthesiophyten nahmen nicht zu, während die Knochenmasse im distalen Radius nach 24 Wochen signifikant (p=0,020) zunahm.
- Bei der PAMPA («Preventing Arthritis in a Multicenter Psoriasis At-risk Cohort») handelt es sich um eine laufende randomisiert-kontrollierte doppelverblindete Multizenter-Studie, in welcher evaluiert werden soll, ob die Behandlung mit dem IL-23-Inhibitor Guselkumab der Progression von subklinischen strukturellen gelenkbezogenen Auffälligkeiten entgegenwirken kann [10,11]. Eingeschlossen werden Patienten mit Plaque-Psoriasis, die ein hohes PsA-Risiko aufweisen. Als koprimärer Endpunkt gilt die Veränderung subklinischer struktureller gelenkbezogener Abnormitäten (gemessen mittels Power-Doppler-Sonografie) von Baseline bis Woche 24 in der Guselkumab-Gruppe vs. der Kontrollgruppe. Die Teilnehmer der Kontrollgruppe erhalten keine Biologika-Therapie.
Beide genannten Biologika – Secukinumab (Cosentyx®) und Guselkumab (Tremfya®) – sind in der Schweiz unter anderem im Indikationsgebiet Psoriasis-Arthritis zugelassen [14].
Fazit
Zusammenfassend handelt es sich bei Patienten mit hohem PsA-Risiko um eine relativ leicht identifizierbare Population. Weltweit befassen sich zahlreiche Forschungsprojekte mit der Früherkennung und -intervention von PsA. Obschon inzwischen gewisse Faktoren eruiert werden konnten, welche bei bestehender Plaque-Psoriasis mit einem erhöhten Risiko für PsA assoziiert sind, besteht ein Bedarf, individuelle PsA-Risikofaktoren akkurater zu evaluieren. Hinsichtlich therapeutischer Interventionen deutet die aktuelle Datenlage darauf hin, dass der Einsatz von Biologika mit hoher Wahrscheinlichkeit das PsA-Risiko reduziert, wobei der adäquate Zeitpunkt für den Therapiebeginn und die involvierten Mechanismen bislang nicht vollständig geklärt sind. Generell stellen sich in Bezug auf PsA-Prävention als Forschungsgegenstand Fragen in Bezug auf Patientenakzeptanz und Ethik von Langzeitstudien. Die Bereitschaft von Psoriasis-Patienten an PsA-Präventionsstudien teilzunehmen sei von verschiedenen Faktoren abhängig, so Prof. Coates [1]. Ein Vorteil bestehe darin, dass viele der Wirksubstanzen, welche hinsichtlich präventiver Effekte auf PsA untersucht werden, auch gegen Plaque-Psoriasis wirksam seien. Aber die Frage wie in längerfristig angelegten randomisierten Studien ein Kontroll-Arm operationalisiert werden kann, sodass es ethisch vertretbar ist, stelle eine grosse Hürde für Langzeitstudienprojekte dar, so die Referentin [1].
Kongress: World Psoriasis & Psoriatic Arthritis Conference
Literatur:
- «Can we prevent psoriatic arthritis?», Keynote lecture, Professor Laura Coates, IFPA Conference, 7th World Psoriasis & Psoriatic Arthritis Conference, 27–29 June 2024, Stockholm.
- Gottlieb AB, et al.: Use of etanercept for psoriatic arthritis in the dermatology clinic: the Experience Diagnosing, Understanding Care, and Treatment with Etanercept (EDUCATE) study. J Dermatolog Treat 2006;17(6): 343–352.
- Eder L, et al.: POS0019 Prediction of Psoriatic Arthritis Tool (PRESTO): Development And Performance Of A New Scoring System For Psoriatic Arthritis Risk. Annals of the Rheumatic Diseases 2023; 82: 215.
- Rudge A, et al. POS0964 Dynamic prediction of Psoriatic Arthritis in a cohort of Psoriasis Patients using UK Primary Care Electronic Health Records. Annals of the Rheumatic Diseases 2024; 83: 699–700.
- «iPROLEPSIS», www.iprolepsis.eu, (letzter Abruf 25.09.2024).
- «PSORCAST Study», www.med.upenn.edu/inflammatory-arthritis/psorcast-study.html, (letzter Abruf 25.09.2024).
- «EU-Forschungsprojekt HIPPOCRATES entwickelt personalisierte Therapieansätze für Menschen mit Psoriasis-Arthritis», www.fau.de/2021/07/news/wissenschaft/eu-projekt-soll-behandlungsmoeglichkeiten-der-psoriasis-arthritis-verbessern, (letzter Abruf 25.09.2024).
- Pennington SR, et al.: Multi-omics Approach to the Identification of Biomarkers for Progression from Psoriasis to Psoriatic Arthritis, Poster, MSACL 2024 14th Annual Conference & Exhibits, March 17–22, 2024. www.msacl.org, (letzter Abruf 25.09.2024).
- Kampylafka E, et al.: Disease interception with interleukin-17 inhibition in high-risk psoriasis patients with subclinical joint inflammation-data from the prospective IVEPSA study. Arthritis Res Ther 2019 Jul 26; 21(1): 178.
- Haberman RH, et al.: Efficacy of guselkumab, a selective IL-23 inhibitor, in Preventing Arthritis in a Multicentre Psoriasis At-Risk cohort (PAMPA): protocol of a randomised, double-blind, placebo controlled multicentre trial. BMJ Open 2022 Dec 23; 12(12): e063650. doi: 10.1136/bmjopen-2022-063650.
- Merola JF, et al.: A clinical review of structural damage in psoriatic arthritis for dermatologists: From pathogenesis to ongoing controversies. Journal of the American Academy of Dermatology 2024; 90(Issue 2) 349–357.
- Scher JU, et al.: Preventing psoriatic arthritis: focusing on patients with psoriasis at increased risk of transition. Nat Rev Rheumatol 2019; 15(3): 153–166.
- Kimak A, et al.: Psoriatic Arthritis: Development, Detection and Prevention: A Scoping Review. Journal of Clinical Medicine. 2023; 12(11): 3850.
www.mdpi.com/2077-0383/12/11/3850#, (letzter Abruf 25.09.2024). - Swissmedic: Arzneimittelinformation, www.swissmedicinfo.ch, (letzter Abruf 26.09.2024).
DERMATOLOGIE PRAXIS 2024; 34(5): 24–26 (veröffentlicht am 28.10.24, ahead of print)
Autoren
- Mirjam Peter, M.Sc.
Publikation
- DERMATOLOGIE PRAXIS


Comments are closed.