Das Lennox-Gastaut-Syndrom und das Dravet-Syndrom sind seltene und schwere entwicklungsbedingte und epileptische Enzephalopathien mit Beginn im Säuglings- oder frühen Kindesalter. Neben den Anfällen treten häufig Komorbiditäten auf, die sowohl für die Patienten als auch ihre Betreuer eine erhebliche physische, finanzielle, soziale und psychische Belastung darstellen. Daher sollte ein modernes Therapiemanagement nicht allein auf die Anfallskontrolle zielen.
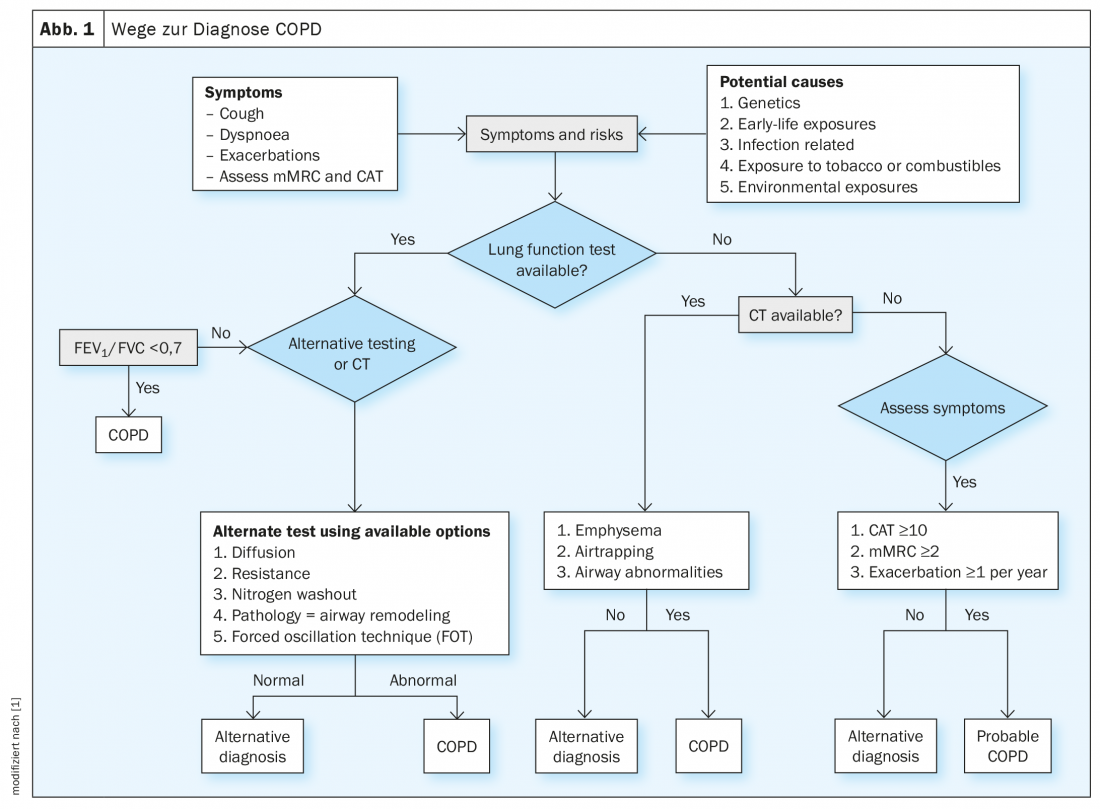
Epilepsie kann sich im Kindesalter unterschiedlich manifestieren. Das Dravet-Syndrom (DS) tritt bereits im Säuglingsalter auf und ist gekennzeichnet durch Infekt-Assoziierte fokale und generalisierte Anfälle. Ein Status epilepticus ist häufig, wodurch oft eine stationäre Notfalltherapie indiziert ist, berichtete Prof. Dr. med. Regina Trollmann, Erlangen (D). Im Laufe der Zeit kann es zu Entwicklungsstörungen und Komorbiditäten kommen. Hierbei konnte eine Korrelation der Anfallshäufigkeit und -schwere mit Komorbiditäten und der Lebensqualität festgestellt werden. Das Lennox-Gastaut Syndrom (LGS) manifestiert sich meist zwischen dem dritten und fünften Lebensjahr und zeichnet sich durch eine schwere epileptische Enzephalopathie (DEE) aus. 90% der Anfälle sind refraktär, sodass das Morbiditäts- und Mortalitätsrisiko deutlich erhöht sind. Als Komorbiditäten treten häufig Verhaltensstörungen, wie beispielsweise Hyperaktivität, Aggression und autistische Züge, Störungen des Schlafzyklus sowie eine eingeschränkte Mobilität auf. Entwicklungs- und epileptische Enzephalopathien sind mit einer hohen Frequenz klinischer Anfälle und interiktaler Anfallsmuster assoziiert – und häufig mit einer Pharmakoresistenz. Bei Kindern mit Epilepsie liegt die Pharmakoresistenz bei 28–36%, so die Expertin.
| Cannabidiol Fertigarznei auf einen Blick |
| Epidyolex® wird als Zusatztherapie von Krampfanfällen im Zusammenhang mit dem Lennox-Gastaut-Syndrom (LGS) oder dem Dravet-Syndrom (DS) in Verbindung mit Clobazam bei Patienten ab 2 Jahren angewendet. |
| Die flexible und schrittweise Dosierung kann ganz auf die Bedürfnisse der Patienten abgestimmt werden. |
| Es konnte bei LGS- und DS-Patienten in einem breiten Spektrum von Anfallstypen und Altersgruppen eine Verbesserung der anfallsbezogenen Ziele nachgewiesen werden. |
| Auch eine Verbesserung der nicht-anfallsbezogenen Ziele wie z.B. Kognition, Verhalten und Kommunikation konnte beobachtet werden. |
| Die Fertigarznei zeichnet sich durch eine langanhaltende und gute Verträglichkeit aus. |
Effektive Behandlung mit Cannabidiol
Eine deutliche Reduktion des Anfallsfrequenz sowohl bei DS als auch LGS konnte in mehreren klinischen Studien für Cannabidiol (CBD), der nicht-psychoaktiven Komponente von Cannabis, nachgewiesen werden. Doch darüber hinaus legen präklinische Daten auch antiinflammatorische und antioxidative Effekte auf verschiedene neurogliale Strukturen sowie Effekte auf das Verhalten nahe. Eine offene Extensionsstudie zeigte zudem, dass es innerhalb von 156 Wochen unter der Behandlung mit Cannabidiol zu einer Reduktion der Sturzanfälle um 48–71% kam. Aktuelle Real-World-Daten belegen nun, dass das moderne Behandlungsmanagement mehr kann, als eine effektive Anfallskontrolle zu generieren. Die BEhavior, COgnition, and More with Epidiolex® (BECOME) war eine 20-minütige Online-Querschnittsbefragung, die mit umfangreichem Input von Pflegekräften, medizinischen Fachkräften und Epilepsieforschern entwickelt wurde und auf Fragen aus validierten Messungen und zuvor veröffentlichten Berichten von Pflegekräften basierte. In den USA ansässige Betreuer von Menschen mit LGS oder DS, die seit ≥3 Monaten mit CBD (Epidiolex®, 100 mg/ml orale Lösung) behandelt wurden, wurden gebeten, den letzten Monat mit dem Zeitraum vor der CBD-Behandlung zu vergleichen und ihren Eindruck von Veränderungen anhand symmetrischer Likert-Skalen zu bewerten. Insgesamt 498 Betreuer (97% Eltern) von Patienten mit LGS (80%) oder DS (20%) füllten die Umfrage aus. Die Patienten nahmen im Median eine CBD-Dosis von 14 mg/kg/d und durchschnittlich gleichzeitig vier Medikamente gegen Anfälle ein. Ein Grossteil der Befragten berichtete über Verbesserungen bei mindestens einer Frage in allen anfallsfreien Bereichen: Wachsamkeit, Kognition und Exekutivfunktion (85%); emotionale Funktion (82%); Sprache und Kommunikation (79% bei nonverbalen und 74% bei verbalen Patienten); Aktivitäten des täglichen Lebens (51%); Schlaf (51%); und körperliche Funktion (46%). Die Befragten berichteten über Verbesserungen in anfallsbezogenen Bereichen, einschliesslich der allgemeinen Anfallshäufigkeit (85%), der allgemeinen Anfallsschwere (76%), der anfallsfreien Tage pro Woche für ≥1 Anfallstyp (67%) und der Anfallsfreiheit im letzten Monat (16%). Die Mehrheit der Befragten, die über eine Verringerung der Anfallshäufigkeit berichteten, meldeten auch Verbesserungen in anfallsfreien Bereichen (5–80%). Verbesserungen in anfallsfreien Bereichen (18–56%) wurden allerdings auch von Patienten berichtet, bei denen sich die Anfallshäufigkeit entweder nicht verändert oder verschlechtert hatte. 93% der Befragten gaben an, die CBD-Behandlung fortsetzen zu wollen. Die Gründe dafür lagen sowohl in der geringeren Anfallsbelastung, als auch in der Verbesserung der nicht-anfallsbezogenen Komorbiditäten, fasste die Expertin zusammen.
Quelle: Pressegespräch «Beyond Seizures – Einblicke in die Therapie schwer zu behandelnder, seltener Epilepsieformen von Kindern und Erwachsenen», 16.05.2024. Jazz Pharmaceuticals.
Weiterführende Literatur:
- Berg AT, Dixon-Salazar T, Meskis MA, et al.: Caregiver-reported outcomes with real-world use of cannabidiol in Lennox-Gastaut syndrome and Dravet syndrome from the BECOME survey. Epilepsy Research 2024; 200: 107280.
- Rosenberg EC, Chamberland S, Bazelot M et al. Cannabidiol modulates excitatory-inhibitory ratio to counter hippocampal hyperactivity. Neuron 2023; 111(8): 1282–1300.e8.
- Patel AD, Mazurkiewicz-Bełdzińska M, Chin RF et al. Long-term safety and efficacy of add-on cannabidiol in patients with Lennox-Gastaut syndrome: Results of a long-term open-label extension trial. Epilepsia 2021; 62(9): 2228–2239.
- EPIDYOLEX® Fachinformation, aktueller Stand. swissmedicinfo.ch.
InFo NEUROLOGIE & PSYCHIATRIE 2024; 22(3): 31
Autoren
- Leoni Burggraf
Publikation
- INFO NEUROLOGIE & PSYCHIATRIE